题目内容
7.下列叙述正确的是( )| A. | 1 mol CO2 的质量为44g/mol | |
| B. | NA个CO2的质量与CO2的相对分子质量数值上相同 | |
| C. | CO2的摩尔质量等于CO2的相对分子质量 | |
| D. | CO2的摩尔质量为44g |
分析 A.质量的单位为g,g/mol为摩尔质量的单位;
B.NA个CO2的质量为44g,CO2的相对分子质量为44;
C.摩尔质量为g/mol为单位时,二者在数值上相等;
D.摩尔质量的单位应该为g/mol.
解答 解:A.1mol二氧化碳的质量为44g,故A错误;
B.NA个CO2的物质的量为1mol,质量为44g,CO2的相对分子质量为44,二者在数值上相同,故B正确;
C.CO2的摩尔质量为44g/mol,CO2的相对分子质量为44,二者的单位不同,故C错误;
D.二氧化碳的摩尔质量为44g/mol,故D错误;
故选B.
点评 本题考查了物质的量的简单计算,题目难度不大,明确质量与摩尔质量、摩尔质量与相对分子质量的区别为解答关键,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
15.欲除去表溶液中的杂质,写出所加试剂(适量)的化学式和有关离子方程式:
| 溶液 | 杂质 | 应加试剂 | 离子方程式 |
| BaCl2 | HCl | ||
| Na2SO4 | Na2CO3 | ||
| FeCl2 | CuCl2 |
2.化学与人们的日常生活密切相关,下列叙述正确的是( )
| A. | 鸡蛋清溶液中加入CuSO4溶液,有沉淀析出,该性质可用于蛋白质的分离与提纯 | |
| B. | 明矾净水时发生了化学及物理变化,能起到杀菌、消毒的作用 | |
| C. | 淀粉溶液、豆浆、碳素墨水均可发生丁达尔现象 | |
| D. | 火柴头的主要成分是氯酸钾和硫单质,分别属于电解质和非电解质 |
12.下列有关离子共存或离子反应的说法,正确的是( )
| A. | 与Al反应能放出H2的溶液中可能大量存在Fe2+、Na+、NO3-、Cl- | |
| B. | 使紫色石蕊变蓝的溶液中可能大量存在Al3+、SO42-、NH4+、CO32- | |
| C. | Al2(SO4)3溶液与氨水的反应:Al3++3OH-=Al(OH)3↓ | |
| D. | FeCl3溶液腐蚀印刷电路板的反应:2Fe3++Cu=2Fe2++Cu2+ |
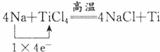 ,氧化剂:TiCl4,还原剂:Na.
,氧化剂:TiCl4,还原剂:Na.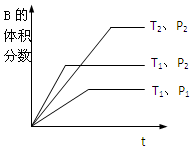 (1)在一定温度下,将2molA和2molB两种气体相混合后于容积为2L的某密闭容器中,发生如下反应3A(g)+B(g)?xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)在一定温度下,将2molA和2molB两种气体相混合后于容积为2L的某密闭容器中,发生如下反应3A(g)+B(g)?xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白: .
.