题目内容
8.在35Cl中含有17个电子,18个中子,氯在周期表中位置第三周期第ⅤⅡA族;.分析 根据原子符号的含义、质子数=原子序数=核外电子、质量数=质子数+中子数;
根据电子层数与其周期数相等,主族元素最外层电子数与其族序数相等判断元素在周期表中位置.
解答 解:35Cl的质子数为17,质量数为35,中子数=35-17=18,核外电子=质子数=18,Cl的质子数为17,核外有3个电子层,最外层电子数为7,其原子结构示意图为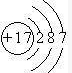 ,位于第三周期第ⅤⅡA族;
,位于第三周期第ⅤⅡA族;
故答案为:17;18;第三周期第ⅤⅡA族;
点评 本题考查原子符号的含义、位置与结构的关系,难度不大,注意知识的积累.

练习册系列答案
相关题目
13.用NA表示阿伏加德罗常数的值.下列说法中,不正确的是( )
| A. | 32g氧气含有2NA个氧原子 | |
| B. | 32g臭氧含有2NA个氧原子 | |
| C. | 32g氧气和臭氧的混合气体中含有2NA个氧原子 | |
| D. | 32g氧气和臭氧的混合气体含有NA个氧原子 |
17.如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是( )
| R | ||
| X | Y | Z |
| A. | Y的氢化物比R的氢化物稳定 | |
| B. | 原子半径大小顺序是Z>Y>X | |
| C. | Y、R形成化合物的化合物YR2能使KMnO4溶液褪色 | |
| D. | X、Z可形成化合物XZ3,且该化合物属离子化合物 |
18.下列物质中,既含有离子键,又含有非极性键的是( )
| A. | Na2O2 | B. | KOH | C. | CaCl2 | D. | CO2 |
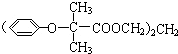 ,可用于降低血液中的胆固醇,该物质合成线路如图所示:
,可用于降低血液中的胆固醇,该物质合成线路如图所示: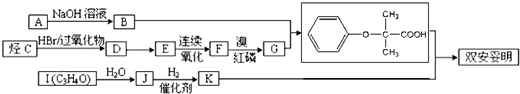
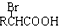 $\stackrel{苯酸钠}{→}$
$\stackrel{苯酸钠}{→}$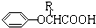
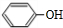 .
.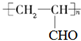
 +K→双安妥明”的化学方程式为
+K→双安妥明”的化学方程式为 .
.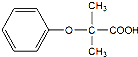 的同分异构体有6种(不考虑立体异构)
的同分异构体有6种(不考虑立体异构)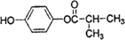 (写结构简式).
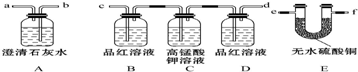
(写结构简式).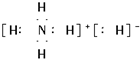 .
.
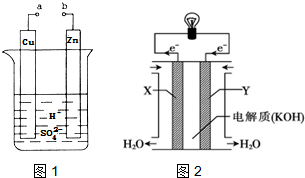
 .
.