题目内容
已知一个N2O3分子的质量为a g,一个N2O5分子的质量为b g,若其中一个氧原子质量的1/16作为相对原子质量的标准,则NO2的相对分子质量为
[ ]
A.8(b+a)/(b-a)
B.16(b+a)/(b-a)
C.8(b-a)/(b+a)
D.16(b-a)/(b+a)
答案:A
解析:
解析:
|
导解:方法一 设N和O的质量分别为x和y, 相对原子质量的标准为氧原子质量的1/16等于(5a-3b)/64,NO2的相对分子质量等于x+2y,一比即得答案. 方法二 从原子组成上看:N2O3+N2O5=N4O8=4NO2,所以NO2的质量为(a+b)/4.N2O |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
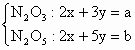 解得:
解得: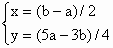
 N2O3=O2=2O,所以氧原子的质量为(b-a)/2,相对原子质量的标准为氧原子质量的1/16等于(b-a)/32,一比即得答案.
N2O3=O2=2O,所以氧原子的质量为(b-a)/2,相对原子质量的标准为氧原子质量的1/16等于(b-a)/32,一比即得答案.


