题目内容
某课外小组欲测定过氧化钠与碳酸钠混合物中过氧化钠的质量分数,准确称量a克样品,下列后续实验方案中,不合理的是( )
| A、与足量水反应并加热,收集到标准状况下V1L干燥气体 |
| B、与足量稀盐酸反应并蒸干,称量剩余固体质量m1g |
| C、隔绝空气加热,冷却后,称量剩余固体质量m2g |
| D、溶于足量水,滴入足量氯化钙溶液,过滤、洗涤、干燥、称重质量为m3g |
考点:化学实验方案的评价
专题:
分析:A.过氧化钠与水反应生成氧气;
B.最终反应生成氯化钠;
C.过氧化钠与碳酸钠都稳定;
D.碳酸钠与氯化钙反应生成碳酸钙沉淀.
B.最终反应生成氯化钠;
C.过氧化钠与碳酸钠都稳定;
D.碳酸钠与氯化钙反应生成碳酸钙沉淀.
解答:
解:A.过氧化钠与水反应生成氧气,可能为V1 L,故A正确;
B.最终反应生成氯化钠,质量变化,故B正确;
C.过氧化钠与碳酸钠都稳定,不易分解,故C错误;
D.碳酸钠与氯化钙反应生成碳酸钙沉淀,根据碳酸钙的质量确定过氧化钠的质量,故D正确.
故选C.
B.最终反应生成氯化钠,质量变化,故B正确;
C.过氧化钠与碳酸钠都稳定,不易分解,故C错误;
D.碳酸钠与氯化钙反应生成碳酸钙沉淀,根据碳酸钙的质量确定过氧化钠的质量,故D正确.
故选C.
点评:本题考查化学实验方案的评价,为高频考点,侧重实验基本操作和实验原理的考查,题目难度不大.

练习册系列答案
相关题目
在无色溶液中能大量共存的离子组是( )
| A、Ca2+、Cl-、CO32- |
| B、K+、Na+、SO42- |
| C、HCO3-、Na+、OH- |
| D、K+、Fe3+、SCN- |
体积相同的盐酸和醋酸两溶液中n(Cl-)=n(CH3COO-)=0.01mol,下列正确的是( )
| A、两种溶液的pH不相同 |
| B、它们与NaOH完全中和时,醋酸溶液所消耗的NaOH多 |
| C、分别用水稀释相同倍数时,n(Cl-)=n(CH3COO-) |
| D、它们分别与足量CaCO3反应时,放出的CO2一样多 |
检查烧碱中是否混有纯碱的正确方法是( )
| A、加热看是否有气体生成 |
| B、滴入盐酸后看是否有气体生成 |
| C、溶解后检查溶液的酸碱性 |
| D、灼烧看火焰是否为黄色 |
如图所示是配制一定物质的量浓度溶液的过程示意图.下列说法中错误的是( )
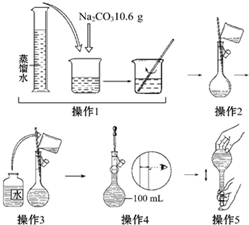

| A、所配制的Na2CO3溶液的物质的量浓度为1.0 mol?L-1 |
| B、操作2是将溶解的Na2CO3溶液转移到容量瓶中 |
| C、操作4如果仰视,结果配得溶液浓度偏低 |
| D、操作5中,定容摇匀后发现液面低于刻度线,要继续加水至液面与刻度线平齐 |
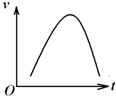 氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl-的速率v(纵坐标)与反应时间t(横坐标)的关系如图所示,已知该反应速率随着溶液中c(H+)的增大而加快.
氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl-的速率v(纵坐标)与反应时间t(横坐标)的关系如图所示,已知该反应速率随着溶液中c(H+)的增大而加快.