题目内容
7.决定化学反应速率的最主要因素是( )| A. | 反应物浓度 | B. | 反应温度 | ||
| C. | 反应物自身的性质 | D. | 是否使用催化剂 |
分析 影响化学反应速率的因素很多,物质本身的性质是决定性的因素,温度、压强、浓度、催化剂、固体表面积是外界因素.
解答 解:影响化学反应速率的因素中,反应物的结构与性质是决定性的因素,即最主要因素,而温度、浓度、压强、催化剂等为次要因素.
故选C.
点评 本题考查学生影响化学反应速率的因素,为高频考点,注意反应物的结构与性质是决定性的因素这一点是关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列化学反应中,反应物总能量高于生成物总能量的是( )
| A. | 铝片和稀盐酸反应 | B. | 氢氧化钡晶体和氯化铵反应 | ||
| C. | 灼热的碳与CO2反应 | D. | 甲烷在氧气中燃烧 |
17.下列对各组物质性质的比较中,正确的是( )
| A. | 沸点:HF<HCl | B. | 熔点:Al>Na | C. | 密度:H2O>MgCl2 | D. | 硬度:C<Si |
12.用锌与稀硫酸反应制H2时,下列能延缓反应速率但又不影响生成氢气总量的是( )
| A. | 加入少量NaNO3溶液 | B. | 加入少量CuSO4溶液 | ||
| C. | 加入少量CH3COONa固体 | D. | 改用98%的浓硫酸 |
19.只用一种试剂就能区别乙醇、乙酸和葡萄糖三种溶液,该试剂是( )
| A. | 金属钠 | B. | 石蕊溶液 | ||
| C. | 新制的氢氧化铜悬浊液 | D. | NaHCO3溶液 |

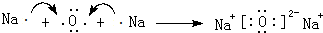 .
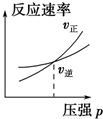
.
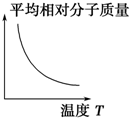
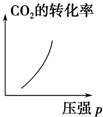
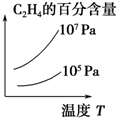
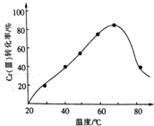 工业含铬废水的处理原理是将CrO32-转化为Cr3+,再将Cr3+转化为Cr(OH)3沉淀,利用硫酸工业废气中的SO2处理含铬废水,既充分利用资源,以废治废,还能节约生成本.
工业含铬废水的处理原理是将CrO32-转化为Cr3+,再将Cr3+转化为Cr(OH)3沉淀,利用硫酸工业废气中的SO2处理含铬废水,既充分利用资源,以废治废,还能节约生成本.