题目内容
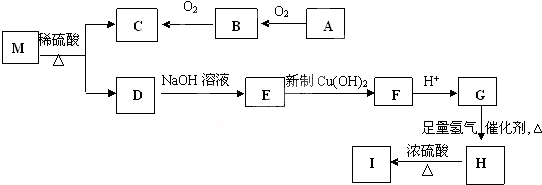
在元素周期表中,一稀有气体元素原子的最外层电子构型为4s24p6,与其同周期的A、B、C、D四种元素,它们的原子的最外层电子数依次为2、1、1、7,其中A、C两元素原子的次外层电子数为8,B、D两元素原子的次外层电子数18,E、D两元素处于同族,且在该族元素中,E的气态氢化物的沸点最高,E、F、G、H四种元素处于同一周期,F的最高价氧化物对应的水化物酸性在同周期中是最强的,G的电离能介于E、F之间,H与F相邻.
(1)B元素在周期表中的位置 ,B元素基态原子的电子排布式为 .
(2)A、C、D三种元素形成的简单离子的半径由大到小的顺序是(写离子符号) .
(3)E、F、G三种元素的第一电离能由大到小的顺序是(写元素符号) .
(4)H的气态氢化物分子空间结构为直线形,则H原子杂化类型是 ,分子中σ键和π键个数比为 .
(5)物质[B(NH3)4]SO4中,B离子与NH3分子之间形成 键.
(6)H和F形成一种超硬、耐磨、耐高温的新型化合物,该化合物属于 晶体.
(1)B元素在周期表中的位置
(2)A、C、D三种元素形成的简单离子的半径由大到小的顺序是(写离子符号)
(3)E、F、G三种元素的第一电离能由大到小的顺序是(写元素符号)
(4)H的气态氢化物分子空间结构为直线形,则H原子杂化类型是
(5)物质[B(NH3)4]SO4中,B离子与NH3分子之间形成
(6)H和F形成一种超硬、耐磨、耐高温的新型化合物,该化合物属于
考点:位置结构性质的相互关系应用
专题:
分析:在元素周期表中,一稀有气体元素原子的最外层电子构型为4s24p6,与其同周期的A、B、C、D四种元素,则A、B、C、D为第四周期元素,它们的原子的最外层电子数依次为2、1、1、7,其中A、C两元素原子的次外层电子数为8,则A为钙元素,C为钾元素,B、D两元素原子的次外层电子数18,则B为铜元素,D为为溴元素,E、D两元素处于同族,且在该族元素中,E的气态氢化物的沸点最高,则E为氟元素,E、F、G、H四种元素处于同一周期,F的最高价氧化物对应的水化物酸性在同周期中是最强的,则F为氮元素,G的电离能介于E、F之间,则G为氧元素,H与F相邻,则H为碳元素,据此答题.
解答:
解:在元素周期表中,一稀有气体元素原子的最外层电子构型为4s24p6,与其同周期的A、B、C、D四种元素,则A、B、C、D为第四周期元素,它们的原子的最外层电子数依次为2、1、1、7,其中A、C两元素原子的次外层电子数为8,则A为钙元素,C为钾元素,B、D两元素原子的次外层电子数18,则B为铜元素,D为为溴元素,E、D两元素处于同族,且在该族元素中,E的气态氢化物的沸点最高,则E为氟元素,E、F、G、H四种元素处于同一周期,F的最高价氧化物对应的水化物酸性在同周期中是最强的,则F为氮元素,G的电离能介于E、F之间,则G为氧元素,H与F相邻,则H为碳元素,
(1)B为铜元素,在周期表中第4周期第ⅠB族,铜是29号元素,基态原子的电子排布式为[Ar]3d104s1,故答案为:第4周期第ⅠB族;[Ar]3d104s1;
(2)根据元素周期律,电子层数多,微粒半径大,电子层数相同时,核电荷数多,半径小,所以Ca2+、K+、Br-三种离子的半径由大到小的顺序是Br->K+>Ca2+,故答案为:Br->K+>Ca2+;
(3)同周期元素,从左向右第一电离能逐渐增大,但由于氮原子最外层p轨道上是半满状态,所以它的第一电离能高于相邻主族元素,所以F、N、O三种元素的第一电离能由大到小的顺序是F>N>O,故答案为:F>N>O;
(4)H的气态氢化物分子空间结构为直线形分子为C2H2,在分子中C2H2,C原子杂化是sp杂化,分子中有3个σ键和2个π键,所以它们个数比为 3:2,故答案为:sp;3:2;
(5)B为铜元素,[Cu(NH3)4]SO4中,铜离子有空轨道,NH3分子中的氮原子上有孤电子对,铜离子和氨分子之间形成配位键,故答案为:配位;
(6)C和N形成一种超硬、耐磨、耐高温的新型化合物,该化合物属于原子晶体,故答案为:原子.
(1)B为铜元素,在周期表中第4周期第ⅠB族,铜是29号元素,基态原子的电子排布式为[Ar]3d104s1,故答案为:第4周期第ⅠB族;[Ar]3d104s1;
(2)根据元素周期律,电子层数多,微粒半径大,电子层数相同时,核电荷数多,半径小,所以Ca2+、K+、Br-三种离子的半径由大到小的顺序是Br->K+>Ca2+,故答案为:Br->K+>Ca2+;
(3)同周期元素,从左向右第一电离能逐渐增大,但由于氮原子最外层p轨道上是半满状态,所以它的第一电离能高于相邻主族元素,所以F、N、O三种元素的第一电离能由大到小的顺序是F>N>O,故答案为:F>N>O;
(4)H的气态氢化物分子空间结构为直线形分子为C2H2,在分子中C2H2,C原子杂化是sp杂化,分子中有3个σ键和2个π键,所以它们个数比为 3:2,故答案为:sp;3:2;
(5)B为铜元素,[Cu(NH3)4]SO4中,铜离子有空轨道,NH3分子中的氮原子上有孤电子对,铜离子和氨分子之间形成配位键,故答案为:配位;
(6)C和N形成一种超硬、耐磨、耐高温的新型化合物,该化合物属于原子晶体,故答案为:原子.
点评:本题主要考查了位、构、性之间的关系,涉及到原子核外电子排布、离子半径、第一电离能、化学键、配合物、晶体性质等知识点,解题的关键在于根据信息确定元素的种类,中等难度.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
实验中需2mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别是( )
| A、1000mL,212g |
| B、950mL,543.4g |
| C、任意规格,572g |
| D、1000mL,286g |
下列离子方程式不正确的是( )
| A、将一小粒金属钠放入水中:2Na+2H2O=2Na++2OH-+H2↑ |
| B、将氯气通入氢氧化钠溶液中:Cl2+2OH-=C1-+C1O-+H2O |
| C、向CuSO4溶液中加入适量Ba(OH)2溶液:Ba2++SO42-=BaSO4↓ |
| D、氯气通入水中:Cl2+H2O?H++HClO+Cl- |