题目内容
下列叙述正确的是( )
| A、浓度均为0.1mol?L-1的下列溶液,pH由大到小的排列顺序为:NaOH>Na2CO3>(NH4)2SO4>NaHSO4 |
| B、为确定H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C、常温下,将pH=3的醋酸溶液稀释到原体积的10倍,稀释后溶液的pH=4 |
| D、常温下KSP(AgCl)=1.5×10-4,此时将足量氯化银固体分别投入相同体积的①蒸馏水②0.1mol/L盐酸③0.1mol/L氯化镁溶液④0.1mol/L硝酸银溶液中,则溶液中Ag+浓度:①>④=②>③ |
考点:弱电解质在水溶液中的电离平衡,pH的简单计算
专题:电离平衡与溶液的pH专题
分析:A.强碱溶液pH最大,强酸性溶液pH最小,强碱弱酸盐溶液呈弱酸性,强酸弱碱盐溶液呈弱酸性;
B.NaHA溶液的pH<7,H2A不一定是强酸;
C.醋酸是弱电解质,加水稀释促进醋酸电离;
D.含有银离子或氯离子的物质抑制氯化银溶解,银离子或氯离子浓度越大其抑制能力越强.
B.NaHA溶液的pH<7,H2A不一定是强酸;
C.醋酸是弱电解质,加水稀释促进醋酸电离;
D.含有银离子或氯离子的物质抑制氯化银溶解,银离子或氯离子浓度越大其抑制能力越强.
解答:
解:A.硫酸氢钠能完全电离出氢离子,所以其溶液呈强酸性,氢氧化钠为强碱,碳酸钠为强碱弱酸盐,其溶液呈弱碱性,硫酸铵为强酸弱碱盐,其溶液呈弱酸性,所以这几种溶液PH大小顺序是NaOH>Na2CO3>(NH4)2SO4>NaHSO4,故A正确;
B.NaHA溶液的pH<7,H2A不一定是强酸,如亚硫酸氢钠溶液呈酸性,但亚硫酸是弱酸,故B错误;
C.醋酸是弱电解质,加水稀释促进醋酸电离,所以将pH=3的醋酸溶液稀释到原体积的10倍,稀释后溶液中氢离子浓度大于原来的十分之一,所以溶液的pH<4,故C错误;
D.含有银离子或氯离子的物质抑制氯化银溶解,银离子或氯离子浓度越大其抑制能力越强,所以等浓度的氯化镁溶液比氯化钠溶液中氯化银的溶解性小,硝酸银为可溶性物质,银离子浓度最大,所以银离子浓度大小顺序是④>①>②>③,故D错误;
故选A.
B.NaHA溶液的pH<7,H2A不一定是强酸,如亚硫酸氢钠溶液呈酸性,但亚硫酸是弱酸,故B错误;
C.醋酸是弱电解质,加水稀释促进醋酸电离,所以将pH=3的醋酸溶液稀释到原体积的10倍,稀释后溶液中氢离子浓度大于原来的十分之一,所以溶液的pH<4,故C错误;
D.含有银离子或氯离子的物质抑制氯化银溶解,银离子或氯离子浓度越大其抑制能力越强,所以等浓度的氯化镁溶液比氯化钠溶液中氯化银的溶解性小,硝酸银为可溶性物质,银离子浓度最大,所以银离子浓度大小顺序是④>①>②>③,故D错误;
故选A.
点评:本题考查了弱电解质的电离、难溶物的溶解平衡、盐类水解等知识点,综合性较强,根据弱电解质电离特点、难溶物溶解的影响因素、盐类水解特点来分析解答即可,易错选项是A,注意硫酸氢钠在熔融状态下和水溶液里电离方式的不同,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 有多种同分异构体,其中符合属于酯类并含有苯环的同分异构体有多少种(不考虑立体异构)( )
有多种同分异构体,其中符合属于酯类并含有苯环的同分异构体有多少种(不考虑立体异构)( )| A、6种 | B、5种 | C、4种 | D、3种 |
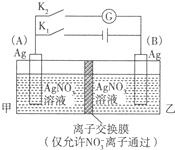 利用如图装置进行实验,甲乙两池均为1mol?L-1的AgNO3溶液,A、B均为Ag电极.实验开始先闭合K1,断开K2.一段时间后,断开K1,闭合K2,形成浓差电池,电流计指针偏转(Ag+浓度越大氧化性越强).下列说法不正确的是( )
利用如图装置进行实验,甲乙两池均为1mol?L-1的AgNO3溶液,A、B均为Ag电极.实验开始先闭合K1,断开K2.一段时间后,断开K1,闭合K2,形成浓差电池,电流计指针偏转(Ag+浓度越大氧化性越强).下列说法不正确的是( )| A、闭合K1,断开K2后,A电极增重 |
| B、闭合K1,断开K2后,乙池溶液浓度上升 |
| C、断开K1,闭合K2后,NO3-向B电极移动 |
| D、断开K1,闭合K2后,A电极发生氧化反应 |
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.如图为RFC工作原理示意图,有关说法正确的是( )


| A、当d极消耗2g H2 时,a极周围会产生22.4L H2 |
| B、电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极 |
| C、c极上发生的电极反应是:O2+2H2O+4e-=4OH- |
| D、c极上进行还原反应,B中的H+可以通过隔膜进入A |
硼的原子序数为5,硼的最高价含氧酸的化学式不可能是( )
| A、HBO2 |
| B、H3BO3 |
| C、H2BO3 |
| D、H4B2O5 |
一定条件下,在体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)?Z(g)△H<0,反应经60s达到平衡并生成0.3mol Z,则下列说法中正确的是( )
| A、以Y浓度变化表示的反应速率为0.0005mol/(L?s) | ||
B、其他条件不变,将容器体积扩大至20L,则Z的平衡浓度变为原来的
| ||
| C、其他条件不变,将容器体积缩小至5L,平衡正向移动,平衡常数增大 | ||
| D、其他条件不变,升高温度逆反应速率加快,正反应速率减慢 |

 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ?mol-1)的变化.
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ?mol-1)的变化. 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇: