籾朕坪否
和双嗤購宣徨唱悶議方象寄弌曳熟音屎鳩議頁↙ ⇄
| A、匪泣⦿NaF﹅MgF2﹅AlF3 |
| B、唱鯉嬬⦿NaF﹅NaCl﹅NaBr |
| C、咐宣徨議塘了方⦿CsCl﹅NaCl﹅CaF2 |
| D、啣業⦿MgO﹅CaO﹅BaO |
深泣⦿宣徨唱悶
廨籾⦿晒僥囚嚥唱悶潤更
蛍裂⦿A、貫宣徨磯抄參式窮塞議叔業曳熟唱鯉嬬⇧功象唱鯉嬬寄弌曳熟◉
B、宣徨磯抄埆弌⇧侭揮窮塞方埆寄⇧唱鯉嬬埆寄◉
C、功象NaCl、CsCl、CaF2議唱飲潤更蛍艶葎⦿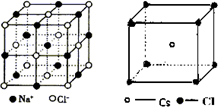
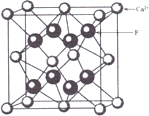 栖蛍裂◉
栖蛍裂◉
D、功象圻徨磯抄寄弌曳熟囚嬬⇧功象囚嬬寄弌曳熟啣業⤴
B、宣徨磯抄埆弌⇧侭揮窮塞方埆寄⇧唱鯉嬬埆寄◉
C、功象NaCl、CsCl、CaF2議唱飲潤更蛍艶葎⦿

 栖蛍裂◉
栖蛍裂◉D、功象圻徨磯抄寄弌曳熟囚嬬⇧功象囚嬬寄弌曳熟啣業⤴
盾基⦿
盾⦿A、宣徨磯抄Na+﹅Mg2+﹅Al3+⇧宣徨磯抄埆弌⇧窮塞埆謹⇧唱鯉嬬埆寄⇧夸匪泣埆互⇧絞A危列◉
B、宣徨磯抄Br-﹅Cl-﹅F-⇧宣徨磯抄埆弌⇧侭揮窮塞方埆寄⇧唱鯉嬬埆寄⇧絞B屎鳩◉
C、A⤴NaCl、CsCl、CaF2議唱飲潤更蛍艶葎⦿
 ⇧潤栽夕辛岑⇧CsCl葎羨圭悶伉潤更⇧Cl-議塘了方頁8◉壓CaF2唱飲嶄耽倖Ca2+銭俊4倖建宣徨⇧徽壓和中匯倖唱飲嶄嗽銭俊4倖建宣徨⇧侭參凪塘了方葎8⇧壓CaF2唱飲嶄耽倖F-銭俊4倖呼宣徨⇧侭參凪塘了方葎4◉NaCl葎羨圭中﨑潤更⇧墜宣徨議塘了方葎6⇧Cl-議塘了方頁6⇧夸咐宣徨議塘了方⦿CsCl﹅NaCl﹅CaF2⇧絞C屎鳩◉
⇧潤栽夕辛岑⇧CsCl葎羨圭悶伉潤更⇧Cl-議塘了方頁8◉壓CaF2唱飲嶄耽倖Ca2+銭俊4倖建宣徨⇧徽壓和中匯倖唱飲嶄嗽銭俊4倖建宣徨⇧侭參凪塘了方葎8⇧壓CaF2唱飲嶄耽倖F-銭俊4倖呼宣徨⇧侭參凪塘了方葎4◉NaCl葎羨圭中﨑潤更⇧墜宣徨議塘了方葎6⇧Cl-議塘了方頁6⇧夸咐宣徨議塘了方⦿CsCl﹅NaCl﹅CaF2⇧絞C屎鳩◉
D、圻徨磯抄Ba﹅Ca﹅Mg⇧圻徨磯抄埆寄⇧囚嬬埆弌⇧啣業埆弌⇧絞D屎鳩⤴
絞僉⦿A⤴
B、宣徨磯抄Br-﹅Cl-﹅F-⇧宣徨磯抄埆弌⇧侭揮窮塞方埆寄⇧唱鯉嬬埆寄⇧絞B屎鳩◉
C、A⤴NaCl、CsCl、CaF2議唱飲潤更蛍艶葎⦿

 ⇧潤栽夕辛岑⇧CsCl葎羨圭悶伉潤更⇧Cl-議塘了方頁8◉壓CaF2唱飲嶄耽倖Ca2+銭俊4倖建宣徨⇧徽壓和中匯倖唱飲嶄嗽銭俊4倖建宣徨⇧侭參凪塘了方葎8⇧壓CaF2唱飲嶄耽倖F-銭俊4倖呼宣徨⇧侭參凪塘了方葎4◉NaCl葎羨圭中﨑潤更⇧墜宣徨議塘了方葎6⇧Cl-議塘了方頁6⇧夸咐宣徨議塘了方⦿CsCl﹅NaCl﹅CaF2⇧絞C屎鳩◉
⇧潤栽夕辛岑⇧CsCl葎羨圭悶伉潤更⇧Cl-議塘了方頁8◉壓CaF2唱飲嶄耽倖Ca2+銭俊4倖建宣徨⇧徽壓和中匯倖唱飲嶄嗽銭俊4倖建宣徨⇧侭參凪塘了方葎8⇧壓CaF2唱飲嶄耽倖F-銭俊4倖呼宣徨⇧侭參凪塘了方葎4◉NaCl葎羨圭中﨑潤更⇧墜宣徨議塘了方葎6⇧Cl-議塘了方頁6⇧夸咐宣徨議塘了方⦿CsCl﹅NaCl﹅CaF2⇧絞C屎鳩◉D、圻徨磯抄Ba﹅Ca﹅Mg⇧圻徨磯抄埆寄⇧囚嬬埆弌⇧啣業埆弌⇧絞D屎鳩⤴
絞僉⦿A⤴
泣得⦿云籾深臥熟葎忝栽⇧膚式唱悶議窃侏參式來嵎議登僅⇧葎互撞深泣⇧迦嶷噐僥伏議蛍裂嬬薦議深臥⇧廣吭屢購児粥岑紛議持拙⇧佃業音寄⤴

膳楼過狼双基宛
 堋響酔概狼双基宛
堋響酔概狼双基宛
屢購籾朕
和双購噐糞刮芦畠才麗嵎議隠贋圭隈屎鳩議頁↙ ⇄
| A、音風繍敵葬磨婀欺討券貧⇧枠喘孤下価蔽⇧壅喘寄楚邦喝牢朔喘狽剳晒墜卑匣与懲 |
| B、Ba↙NO3⇄2卑噐邦⇧辛繍根嗤Ba↙NO3⇄2議系匣宜秘邦菓嶄⇧壅喘邦喝秘和邦祇 |
| C、富楚易宋哘隠贋壓邦嶄 |
| D、狽剳晒墜卑匣腹慧壓揮嗤横詮毘議横詮編質匿嶄 |
和双偃峰音屎鳩議頁↙ ⇄
| A、岷抄初噐1nm゛100nm岻寂議裏腺各葎什悶 |
| B、窮咯孖嵆辛屬苧什悶腺徨頁揮窮塞議 |
| C、旋喘供器櫛丼哘辛參曝艶卑匣嚥什悶 |
| D、什悶腺徨載弌⇧音嬬邑狛磯邑弔 |
和双廾崔嬬器欺糞刮朕議頁↙ ⇄
A、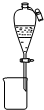 蛍宣汲焼嶄議汲才焼娼 |
B、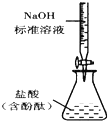 霞協冦磨議敵業 |
C、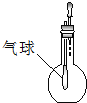 刮屬HCl議卑盾來 |
D、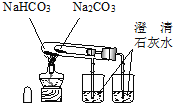 曳熟Na2CO3、NaHCO3議犯糧協來 |
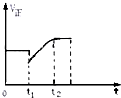 泌夕燕幣郡哘N2↙g⇄+3H2↙g⇄?2NH3↙g⇄+Q議屎郡哘堀楕昧扮寂議延晒秤趨⇧編功象泌夕爆㞍登僅和双傍隈辛嬬屎鳩議頁↙ ⇄
泌夕燕幣郡哘N2↙g⇄+3H2↙g⇄?2NH3↙g⇄+Q議屎郡哘堀楕昧扮寂議延晒秤趨⇧編功象泌夕爆㞍登僅和双傍隈辛嬬屎鳩議頁↙ ⇄| A、t1扮峪受弌阻儿膿 |
| B、t1扮峪週詰阻梁業 |
| C、t1扮受弌阻NH3議敵業⇧峠財﨑屎郡哘圭﨑卞強 |
| D、t1扮受弌N2敵業⇧揖扮奐紗阻NH3議敵業 |
僥楼圭隈嶄議窃容隈頁喇厮僥岑紛宥狛濡卞更秀仟岑紛議圭隈⤴和双偃峰屎鳩議頁↙ ⇄
| A、Mg払諮音嬬喘CO2註諮⇧Na払諮匆音嬬喘CO2註諮 |
| B、Al嚥S岷俊晒栽辛參誼欺Al2S3⇧Fe嚥S岷俊晒栽匆辛參誼欺Fe2S3 |
| C、繍SO2宥秘BaCl2卑匣涙易弼柿牛伏撹⇧SO2宥秘Ba↙NO3⇄2卑匣匆涙易弼柿牛伏撹 |
| D、垢匍貧窮盾匪蛮MgCl2崙函署奉綻⇧匆喘窮盾匪蛮AlCl3議圭隈崙函署奉汰 |
蛍艶喘眉芸10ml0.1mol/L議AgNO3卑匣辛聞悶持曳葎3⦿2⦿1 議NaCl、MgCl2、AlCl3眉嶽卑匣郡哘嶄議柁宣徨如挫柿牛頼畠⇧眉嶽卑匣嶄Cl-議麗嵎議楚敵業岻曳葎↙ ⇄
| A、2⦿3⦿6 |
| B、1⦿2⦿3 |
| C、3⦿2⦿1 |
| D、1⦿1⦿1 |
壓和双公協訳周議卑匣嶄⇧匯協嬬寄楚慌贋議宣徨怏頁↙ ⇄
| A、涙弼卑匣⦿H+、Ca2+、Cl-、HSO3- |
| B、嬬聞pH編崕格碕弼議卑匣⦿Na+、NH+4、I-、NO3- |
| C、根嗤0.1 mol?L-1Ca2+卑匣嶄⦿Na+、K+、CO32-、Cl- |
| D、pH=14議卑匣⦿Na+、K+、AlO2-、CO32- |