题目内容
6.晶体硅是一种重要的非金属材料,模拟制备纯硅的主要步骤如下:②高温下用碳还原二氧化硅制得粗硅
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl$\frac{\underline{\;300℃\;}}{\;}$SiHCl3+H2,
| 沸点/℃ | |
| SiHCl3 | 33.0 |
| SiCl4 | 57.6 |
| HCl | -84 |
可能用到的信息如下:
已知SiHCl3能与H2O强烈反应,在空气中易自燃;
步骤②中粗硅与HCl反应时会生成少量SiCl4;
请回答下列问题:
(1)粗硅与HCl反应完全后,依据上表所示沸点差异提纯SiHCl3.该提纯方法为分馏.
(2)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):

①依次连接的合理顺序为DBCAE;;
装置D中g管的作用是平衡压强;
装置B中的试剂是浓硫酸;
装置C中的烧瓶加热的目的是使滴入烧瓶中的SiHCl3气化.
②装置A中发生反应的化学方程式为SiHCl3+H2$\frac{\underline{\;1000℃-1100℃\;}}{\;}$Si+3HCl.
③操作时应先打开装置D(C或D)中分液漏斗的旋塞,理由是:因为SiHCl3容易在空气自燃,实验中还要注意先通一段时间H2排尽装置中的空气.
(3)请设计实验证明产品硅中是否含微量铁单质:将产品用稀盐酸溶解,取上层清液后先滴加氯水,再滴加硫氰化钾溶液,溶液显红色.
分析 (1)根据题中数据,采用分馏方法提纯SiHCl3;
(2)①依据实验目的可知:锌与硫酸制备氢气,干燥干燥后通入用热水浴加热SiHCl3,在石英管中反应生成硅和氯化氢,最后进行尾气处理,据此排序;
装置D中g管连接分液漏斗与烧瓶,起平衡压强的作用;浓硫酸干燥氢气;通过水浴加热使滴入烧瓶中的SiHCl3气化,与氢气混合均匀;
②SiHCl3和氢气反应有硅单质生成,根据硅的颜色判断D装置中的颜色变化;反应温度较高,普通玻璃会软化;SiHCl3和H2反应生成硅和氯化氢;
③氢气是可燃性气体,易产生爆炸,为防止安全事故的发生,所以先通一段时间H2,将装置中的空气排尽;
(3)铁能够与氢氧化剂反应生成三价铁离子,三价铁离子遇到硫氰酸钾显红色,据此检验铁元素的存在.
解答 解:(1)SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),由于沸点差别较大,可以通过分馏除去杂质,
故答案为:分馏;
(2)①依据实验目的可知:锌与硫酸制备氢气,干燥干燥后通入用水冷却的SiHCl3,在石英管中反应生成硅和氯化氢,最后进行尾气处理,所以正确的顺序为DBCAE;
装置D中g管连接分液漏斗与烧瓶,起平衡压强的作用;
B装置用于干燥氢气,可用浓硫酸;
通过水浴加热使滴入烧瓶中的SiHCl3气化,与氢气混合均匀,
故答案为:DBCAE;平衡压强(“使分液漏斗中的溶液顺利滴下”也给分);浓硫酸;使滴入烧瓶中的SiHCl3气化;
②高温下,SiHCl3和氢气反应生成硅单质,硅单质是灰黑色固体,所以D装置中的现象是:石英管的内壁附有灰黑色晶体;反应方程式为:SiHCl3+H2$\frac{\underline{\;1000℃-1100℃\;}}{\;}$Si+3HCl,
故答案为:SiHCl3+H2$\frac{\underline{\;1000℃-1100℃\;}}{\;}$Si+3HCl;
③氢气是可燃性气体,易产生爆炸,为防止安全事故的发生,所以先通一段时间H2,将装置中的空气排尽,所以应先打开D;
故答案为:D;因为SiHCl3容易在空气自燃,实验中还要注意先通一段时间H2排尽装置中的空气;
(3)铁能够与氢氧化剂反应生成三价铁离子,三价铁离子遇到硫氰酸钾显红色,要检验铁单质的存在可以:先滴加氯水,再滴加硫氰化钾溶液,溶液显红色;
故答案为:先滴加氯水,再滴加硫氰化钾溶液,溶液显红色.
点评 本题考查了制备方案的设计,题目难度中等,明确实验原理和实验目的是解题关键,注意掌握制备方案的设计与评价方法,试题培养了学生的分析能力及化学实验能力.

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案| A. | 5.6 g 铁粉与足量水蒸气反应,失去的电子数为0.3NA | |
| B. | 制取标准状况下22.4 L Cl2,需转移的电子数为2NA | |
| C. | 2.3 g Na在空气中完全燃烧,失去的电子数为0.1NA | |
| D. | 标准状况下3.36 L HF里含有的原子总数为0.3NA |
| A. | 该溶液中,K+、Ca2+、Cl2、Br -可以大量共存 | |
| B. | 与足量Ca( OH)2溶液反应的离子方程式:Ca2++OH-+HS03═CaS03↓+H20 | |
| C. | 与FeCI3溶液反应的离子方程式:SO32-+2 Fe3++H20═SO42-+2Fe2++2H+ | |
| D. | 能使含I2的淀粉溶液蓝色褪去,说明NaHSO3溶液具有漂白性 |
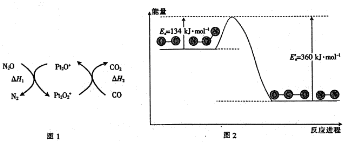
下列说法正确的是( )
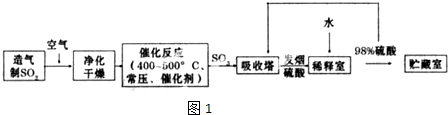
| A. | 由图1可知:△H1=△H+△H2 | |
| B. | 由图2可知△H=-226 kJ/mol | |
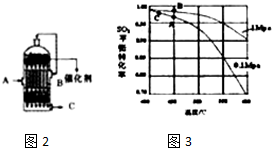
| C. | 为了实现转化需不断向反应器中补充Pt2O+和Pt2O2+ | |
| D. | 由图2可知该反应正反应的活化能大于逆反应的活化能 |

 .
.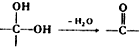
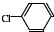 中氯原子较难水解物质A(
中氯原子较难水解物质A( 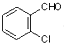 )可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式
)可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式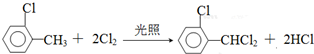 、
、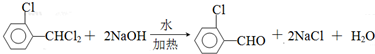 .该合成的第一步主要存在产率低的问题,请写出该步可能存在的有机物杂质的结构简式
.该合成的第一步主要存在产率低的问题,请写出该步可能存在的有机物杂质的结构简式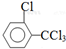 、
、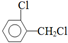 .
.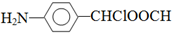 .
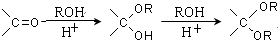
.
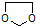 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: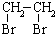
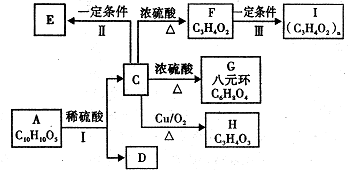
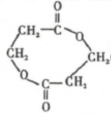 ,反应Ⅲ的化学方程式为
,反应Ⅲ的化学方程式为 .
.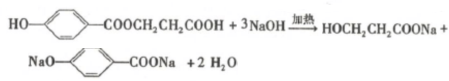 .
.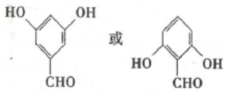 .
.