题目内容
7.对Na2O2+CO2→Na2CO3+O2↑反应的说法不正确的是( )| A. | Na2O2既作氧化剂又作还原剂 | B. | O2是氧化产物 | ||
| C. | 每生成1 mol O2转移4NA个电子 | D. | Na2O2可以作供氧剂 |
分析 由Na2O2+CO2→Na2CO3+O2↑可知,只有过氧化钠中O元素的化合价变化,以此来解答.
解答 解:A.只有过氧化钠中O元素的化合价变化,Na2O2既作氧化剂又作还原剂,故A正确;
B.O元素的化合价升高,失去电子被氧化,对应O2是氧化产物,故B正确;
C.O元素的化合价由-1价升高为0,每生成1 mol O2转移2NA个电子,故C错误;
D.由该反应可知生成氧气,则Na2O2可以作供氧剂,故D正确;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意基本概念的分析,题目难度不大.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案
相关题目
17.下列各组离子,在碱性溶液中能大量共存,且溶液为无色透明的是( )
| A. | K+ MnO4- Cl- SO42- | B. | Na+ Ba2+ NO3- Cl- | ||
| C. | Na+ SO42- Cu2+ Cl- | D. | Na+ H+ NO3- SO42- |
15.某溶液中含有SO32-、SiO32-、CO32-、Na+,向该溶液中通入过量的Cl2,下列判断正确的是( )
①反应前后,溶液中离子浓度基本保持不变的是Na+
②有胶状物质生成
③没有气体产生
④溶液颜色发生变化
⑤只发生了1个氧化还原反应.
①反应前后,溶液中离子浓度基本保持不变的是Na+
②有胶状物质生成
③没有气体产生
④溶液颜色发生变化
⑤只发生了1个氧化还原反应.
| A. | ①②④ | B. | ②③④ | C. | ①③⑤ | D. | ②④⑤ |
2.下列叙述正确的是( )
| A. | 标准状况下,22.4L 的己烷含C-H键的数目为14NA | |
| B. | 常温常压下,14g乙烯和甲基丙烯的混合物含原子数为3NA | |
| C. | 78g苯含有C=C双键的数目为3NA | |
| D. | 15g甲基含有的电子数7NA |
19.新薄荷醇是一种香料,其结构简式为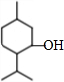 ,新薄荷醇的同分异构体中,羟基连接在
,新薄荷醇的同分异构体中,羟基连接在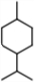 ,不同碳原子上的有(不包括新薄荷醇)( )
,不同碳原子上的有(不包括新薄荷醇)( )
 ,新薄荷醇的同分异构体中,羟基连接在
,新薄荷醇的同分异构体中,羟基连接在 ,不同碳原子上的有(不包括新薄荷醇)( )
,不同碳原子上的有(不包括新薄荷醇)( )| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
6.用下列反应制取O2的过程中:①KClO3(MnO2)分解 ②Na2O2加水 ③HgO分解④H2O2加热 ⑤KMnO2分解,若制得等质量的O2,电子转移数目之比依次是( )
| A. | 1:1:1:1:1 | B. | 2:1:2:1:2 | C. | 3:2:1:2:4 | D. | 1:2:1:2:1 |