题目内容
实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO═3H++6H2O+(CH2)6N4H+[滴定时,1mol (CH2)6N4H+与1mol H+相当],然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ称取1.500g样品,加水溶解,配成250mL溶液.
步骤Ⅱ用酸式滴定管量取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液.用0.1010mol?L-1的NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据实验步骤填空:
①步骤Ⅰ中用到的主要玻璃仪器有 ;
②步骤Ⅱ中酸式滴定管用蒸馏水洗涤后,直接加入样品溶液进行量取,则测得样品中氮质量分数 (填“偏高”、“偏低”或“无影响”,下同).锥形瓶用蒸馏水洗涤后,水未倒尽,则对滴定时用去NaOH标准溶液的体积 .滴定时对NaOH标准溶液体积,读取初读数时仰视,读取终读数时姿势正确,则测得样品中氮质量分数 .
③滴定时边滴边摇动锥形瓶,眼睛应观察
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由 色变成 色.
(2)滴定结果如表所示:
则消耗NaOH标准溶液的体积平均为 mL,该样品中氮的质量分数为 .
步骤Ⅰ称取1.500g样品,加水溶解,配成250mL溶液.
步骤Ⅱ用酸式滴定管量取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液.用0.1010mol?L-1的NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据实验步骤填空:
①步骤Ⅰ中用到的主要玻璃仪器有
②步骤Ⅱ中酸式滴定管用蒸馏水洗涤后,直接加入样品溶液进行量取,则测得样品中氮质量分数
③滴定时边滴边摇动锥形瓶,眼睛应观察
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由
(2)滴定结果如表所示:
| 滴定次数 | 待测溶液体积/mL | 标准NaOH溶液体积读数(mL) | |
| 滴定前/mL | 滴定后/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 2.30 | 22.30 |
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:(1)①配制一定体积的溶液需要用容量瓶来定容,据此选择和合适的玻璃仪器;
②滴定管需要用要盛放的溶液润洗,否则会导致溶液浓度偏低,锥形瓶内是否有水,对实验结果无影响,可从物质的物质的量的角度分析;滴定时眼睛应注意注意观察颜色变化,以确定终点;
③滴定过程中,眼睛要始终注视锥形瓶中溶液颜色的变化;
④根据酚酞的变色范围确定滴定终点时颜色变化;
(2)标准溶液的体积应取三次实验的平均值,计算出溶液中H+的物质的量,根据方程式可知(CH2)6N4H+的物质的量,进而确定样品中氮的质量分数.
②滴定管需要用要盛放的溶液润洗,否则会导致溶液浓度偏低,锥形瓶内是否有水,对实验结果无影响,可从物质的物质的量的角度分析;滴定时眼睛应注意注意观察颜色变化,以确定终点;
③滴定过程中,眼睛要始终注视锥形瓶中溶液颜色的变化;
④根据酚酞的变色范围确定滴定终点时颜色变化;
(2)标准溶液的体积应取三次实验的平均值,计算出溶液中H+的物质的量,根据方程式可知(CH2)6N4H+的物质的量,进而确定样品中氮的质量分数.
解答:
解:(1)①称取1.500g样品,加水溶解,配成250mL溶液,需要的仪器有:天平、250 mL容量瓶、胶头滴管、烧杯、玻璃棒,玻璃仪器有:250 mL容量瓶、胶头滴管、烧杯、玻璃棒,故答案为:250mL容量瓶、胶头滴管、烧杯、玻璃棒;
②酸式滴定管用蒸馏水洗涤后需要再用溶液润洗,否则相当于溶液被稀释,滴定消耗的体积会偏低,测得样品中氮的质量分数也将偏低,锥形瓶用蒸馏水洗涤后,虽然水未倒尽,但待测液中的H+的物质的量不变,则滴定时所需NaOH标准溶液中的氢氧化钠的物质的量就不变,也就是无影响,
滴定时对NaOH标准溶液体积,读取初读数时仰视,读取终读数时姿势正确,则NaOH标准溶液体积会偏小,测得样品中氮质量分数会偏低,故答案为:偏低;无影响;偏低;
③定时边滴边摇动锥形瓶,眼睛应注意观察颜色变化,确定滴定终点,故答案为:B;
④待测液为酸性,酚酞应为无色,当溶液转为碱性时,溶液颜色变为粉红(或浅红),故答案为:无;浅红;
(2)标准溶液的体积应取三次实验的平均值,
首先确定滴定时所用的NaOH标准溶液为
mL=20.00mL,
根据题意中性甲醛溶液一定是过量的,而且1.500g 铵盐 经溶解后,取了其中
进行滴定,即0.15g,
滴定结果,溶液中含有H+(含(CH2)6N4H+)共0.02L××0.1010mol/L=0.00202mol,
根据4NH4++6HCHO═3H++6H2O+(CH2)6N4H+,每生成4molH+(含(CH2)6N4H+),会消耗NH4+4mol,
所以共消耗NH4+0.00202mol,
其中含氮元素0.00202mol×14g/mol=0.02828g
所以氮的质量分数为
×100%=18.85%,
故答案为:20.00mL;18.85%.
②酸式滴定管用蒸馏水洗涤后需要再用溶液润洗,否则相当于溶液被稀释,滴定消耗的体积会偏低,测得样品中氮的质量分数也将偏低,锥形瓶用蒸馏水洗涤后,虽然水未倒尽,但待测液中的H+的物质的量不变,则滴定时所需NaOH标准溶液中的氢氧化钠的物质的量就不变,也就是无影响,
滴定时对NaOH标准溶液体积,读取初读数时仰视,读取终读数时姿势正确,则NaOH标准溶液体积会偏小,测得样品中氮质量分数会偏低,故答案为:偏低;无影响;偏低;
③定时边滴边摇动锥形瓶,眼睛应注意观察颜色变化,确定滴定终点,故答案为:B;
④待测液为酸性,酚酞应为无色,当溶液转为碱性时,溶液颜色变为粉红(或浅红),故答案为:无;浅红;
(2)标准溶液的体积应取三次实验的平均值,
首先确定滴定时所用的NaOH标准溶液为
| (21.03-1.02)+(21.99-2.00)+(22.30-2.30) |
| 3 |
根据题意中性甲醛溶液一定是过量的,而且1.500g 铵盐 经溶解后,取了其中
| 1 |
| 10 |
滴定结果,溶液中含有H+(含(CH2)6N4H+)共0.02L××0.1010mol/L=0.00202mol,
根据4NH4++6HCHO═3H++6H2O+(CH2)6N4H+,每生成4molH+(含(CH2)6N4H+),会消耗NH4+4mol,
所以共消耗NH4+0.00202mol,
其中含氮元素0.00202mol×14g/mol=0.02828g
所以氮的质量分数为
| 0.02828 |
| 0.15 |
故答案为:20.00mL;18.85%.
点评:本题考查物质的含量的测定,侧重于中和滴定的考查,注重于学生实验能力和分析能力和计算能力的综合考查,为考试高频考点,题目难度不大

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
某有机物的分子式为C8H8,经研究表明该有机物不能发生加成反应和加聚反应,在常温下难被酸性KMnO4溶液氧化,但在一定条件下却可与Cl2发生取代反应,而且其一氯代物只有一种.下列对该有机物结构的推断中正确的是( )
| A、该有机物中含有碳碳双键 |
| B、该有机物属于芳香烃 |
| C、该有机物分子含有碳碳叁键 |
| D、该有机物具有三维空间的立体结构 |
2008年是不平凡的一年,有悲痛也有激动,下列说法中有关化学的知识正确的是( )
| A、美丽的“水立方”是北京奥运会游泳馆,设计灵感来自于有机细胞的天然图案以及肥皂泡的形成.在这个中心的蓝色泡墙之内,钢结构的基本单位是一个由12个正五边形和2个正六边形组成的几何细胞,覆盖这个框架的是半透明的“气泡”,称为ETFE,该材料为四氟乙烯(CF2=CF2)与乙烯的共聚物,ETFE属于有机物中的烃类. |
| B、5月12日四川汶川发生特大地震,为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒剂、漂白剂,如:Ca(ClO)2、ClO2、Al(OH)3等. |
| C、美国科学家马丁?查非(Martin Chalfie)、美国华裔化学家钱永健(Roger Tsien)以及日本科学家下村修(Osamu Shimomura)因发现和研究绿色荧光蛋白(green fluorescent protein,GFP)而获2008年度诺贝尔化学奖.向GFP中加入重金属离子,GFP就会变性. |
| D、神舟七号载人飞船于2008年9月25日21点10分发射升空.中国航天员首次空间出舱活动.“神舟七号”的燃料是氢化锂三兄弟--LiH、LiD、LiT.其中Li的质量数为7,这三种物质的化学性质不相同. |
下列反应的离子方程式书写正确的是( )
| A、向明矾溶液中加入等物质的量的Ba(OH)2溶液Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| B、向Fe2(SO4)3溶液中通入足量的H2S:Fe3++H2S=Fe2++S↓+2H+ |
| C、向硝酸银溶液中滴加过量氨水:Ag++2NH3?H2O=[Ag(NH3)2]++2H2O |
| D、含等物质的量的硫酸氢铵与氢氧化钠两种溶液混合:NH4++HSO4-+2OH-=SO42-+NH3↑+2H2O |
已知X、Y两元素能实现如图所示的转化: ,下列说法中错误的是( )
,下列说法中错误的是( )
 ,下列说法中错误的是( )
,下列说法中错误的是( )| A、X可以是金属 |
| B、X可以是非金属 |
| C、m可以等于1或2 |
| D、XYm与XYn的相互转化是可逆反应 |
 铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某不同品牌铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某不同品牌铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.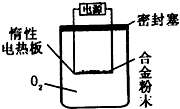


 如图里有6个编号,每个编号代表下列物质中的一种物质,凡用直线连接的相邻两种物质均能发生化学反应,供填写的物质有:a.碳酸钠溶液;b.硫酸镁溶液;C.氯化钡溶液;d.稀硫酸;e.铁;f.硝酸铜溶液,则图中③表示的物质的编号是( )
如图里有6个编号,每个编号代表下列物质中的一种物质,凡用直线连接的相邻两种物质均能发生化学反应,供填写的物质有:a.碳酸钠溶液;b.硫酸镁溶液;C.氯化钡溶液;d.稀硫酸;e.铁;f.硝酸铜溶液,则图中③表示的物质的编号是( )