题目内容
下列离子方程式书写正确的是( )
| A、向CaCl2溶液中通入少量CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+ |
| B、碳酸钠溶液与硫酸氢钠溶液反应:HCO3-+H+=CO2↑+H2O |
| C、向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O |
| D、含有FeBr2溶液中通入足量的Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
考点:离子方程式的书写
专题:离子反应专题
分析:A、向CaCl2溶液中通入少量CO2气体不能发生反应;
B、碳酸钠溶液与硫酸氢钠溶液反应,可以生成碳酸氢根离子,或生成二氧化碳和水;
C、向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全,Ba(OH)2和NH4HSO4,按照1:1反应;
D、含有FeBr2溶液中通入足量的Cl2,碘离子和亚铁离子全部被氧化,离子方程式中亚铁离子和碘离子之比为1:2.
B、碳酸钠溶液与硫酸氢钠溶液反应,可以生成碳酸氢根离子,或生成二氧化碳和水;
C、向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全,Ba(OH)2和NH4HSO4,按照1:1反应;
D、含有FeBr2溶液中通入足量的Cl2,碘离子和亚铁离子全部被氧化,离子方程式中亚铁离子和碘离子之比为1:2.
解答:
解:A、向CaCl2溶液中通入少量CO2气体不能发生反应,故A错误;
B、碳酸钠溶液与硫酸氢钠溶液反应,可以生成碳酸氢根离子,或生成二氧化碳和水,反应的离子方程式CO32-+H+=HCO3-、CO32-+2H+=CO2↑+H2O,故B错误;
C、向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全,Ba(OH)2和NH4HSO4,按照1:1反应,离子方程式为:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O.故C正确;
D、含有FeBr2溶液中通入足量的Cl2,溴离子和亚铁离子全部被氧化,离子方程式中亚铁离子和溴离子之比为1:2,2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-,故D正确;
故选CD.
B、碳酸钠溶液与硫酸氢钠溶液反应,可以生成碳酸氢根离子,或生成二氧化碳和水,反应的离子方程式CO32-+H+=HCO3-、CO32-+2H+=CO2↑+H2O,故B错误;
C、向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全,Ba(OH)2和NH4HSO4,按照1:1反应,离子方程式为:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O.故C正确;
D、含有FeBr2溶液中通入足量的Cl2,溴离子和亚铁离子全部被氧化,离子方程式中亚铁离子和溴离子之比为1:2,2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-,故D正确;
故选CD.
点评:本题考查了离子方程式书写方法和注意问题,主要是量不同产物不同,氧化还原反应的分析判断,注意氯化钙和二氧化碳不反应,题目难度中等.

练习册系列答案
相关题目
古语道:“人要实,火要虚”.此话的意思是说:做人必须脚踏实地,事业才能有成;燃烧固体燃料需要架空,燃烧才能更旺.从燃烧的条件看,“火要虚”的实质是( )
| A、增大可燃物的热值 |
| B、提高空气中氧气的含量 |
| C、提高可燃物的着火点 |
| D、增大可燃物与空气的接触面积 |
下列变化中,不属于化学变化的是( )
| A、用石墨粉打开生锈的铁锁 |
| B、石墨在一定条件下转变为金刚石 |
| C、木炭在高温下还原氧化铜 |
| D、二氧化碳与灼热的炭作用 |
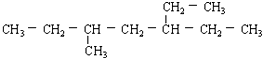 含有一个双键的烯烃,氢化后的产物结构简式为此烃可能有的结构有( )
含有一个双键的烯烃,氢化后的产物结构简式为此烃可能有的结构有( )| A、4种 | B、5种 | C、6种 | D、7种 |
在pH=1的某无色溶液中,下列离子能大量共存的是( )
| A、NH4+、Fe3+、NO3-、CO32- |
| B、Ba2+、NH4+、SO42-、MnO4- |
| C、Na+、Al3+、Cl-、NO3- |
| D、K+、Fe2+、NO3-、SO42- |
下列关于钠的叙述中,不正确的是( )
| A、钠燃烧时发出黄色的火焰 |
| B、钠燃烧时生成氧化钠 |
| C、实验室少量钠需保存在煤油中 |
| D、钠原子的最外层只有一个电子 |