题目内容
 Ⅰ.(1)用14.2g无水硫酸钠配制成500ml溶液,其物质的量浓度为
Ⅰ.(1)用14.2g无水硫酸钠配制成500ml溶液,其物质的量浓度为(2)若从上述溶液中取出10ml,则这10ml 溶液的物质的量浓度为
(3)若将上述10ml 溶液用水稀释到100ml,所得溶液中Na+的物质的量浓度为
Ⅱ.现有36%的醋酸(CH3COOH),密度为1.04g/ml.,欲配制0.1mol/L的醋酸250ml,需要取用36%的醋酸
考点:物质的量浓度的相关计算,配制一定物质的量浓度的溶液
专题:物质的量浓度和溶解度专题
分析:Ⅰ(1)根据n=
计算硫酸钠的物质的量,再根据c=
计算;
(2)溶液是均匀的,取出10mL溶液的浓度与原溶液浓度相等;含有溶质质量为原溶液中的
;
(3)根据稀释定律计算稀释后Na+的物质的量浓度;稀释后硫酸钠的物质的量不变,根据n=cV计算10mL溶液中硫酸钠的物质的量,将稀释后溶液中的SO42-全部沉淀下来,则n(BaCl2)=n(Na2SO4),再根据V=
计算氯化钡溶液的体积;
Ⅱ.根据c=
计算36%的醋酸的物质的量浓度,再根据稀释定律计算需要36%的醋酸的体积;稀释浓溶液配制稀溶液,需要仪器有:量筒,玻璃棒,250mL容量瓶,胶头滴管;定容时仰视,液面在刻度线上方,所配溶液体积偏大,再结合c=
判断.
| m |
| M |
| n |
| V |
(2)溶液是均匀的,取出10mL溶液的浓度与原溶液浓度相等;含有溶质质量为原溶液中的
| 1 |
| 50 |
(3)根据稀释定律计算稀释后Na+的物质的量浓度;稀释后硫酸钠的物质的量不变,根据n=cV计算10mL溶液中硫酸钠的物质的量,将稀释后溶液中的SO42-全部沉淀下来,则n(BaCl2)=n(Na2SO4),再根据V=
| n |
| c |
Ⅱ.根据c=
| 1000ρω |
| M |
| n |
| V |
解答:
解:Ⅰ.(1)14.2g硫酸钠的物质的量=
=0.1mol,溶于水配成500mL溶液,所得溶液物质的量浓度为
=0.2mol/L,故答案为:0.2;
(2)溶液是均匀的,取出10mL溶液的浓度与原溶液浓度相等为0.2mol/L;含有溶质质量为原溶液中的
,含有溶质的质量=14.2g×
=0.284g,故答案为:0.2;0.284;
(3)根据稀释定律,稀释后Na+的物质的量浓度=
=0.04mol/L;稀释后硫酸钠的物质的量不变,10mL溶液中硫酸钠的物质的量=0.2mol/L×0.01L=0.002mol,将稀释后溶液中的SO42-全部沉淀下来,则n(BaCl2)=n(Na2SO4)=0.002mol,需要氯化钡溶液的体积=
=0.02L=20mL,故答案为:0.04;20;
Ⅱ.密度为1.04g/mL、36%的醋酸(CH3COOH)的物质的量浓度=
mol/L=6.24mol/L,欲配制0.1mol/L的醋酸250ml,根据稀释定律,需要取用36%的醋酸体积=
=0.0040L=4.0mL;
稀释浓溶液配制稀溶液,需要仪器有:10mL量筒,玻璃棒,250mL容量瓶,胶头滴管;
定容时仰视,液面在刻度线上方,所配溶液体积偏大,结合c=
可知所配溶液浓度偏小,
故答案为:4.0;10mL量筒;玻璃棒;250mL容量瓶;胶头滴管;偏小.
| 14.2g |
| 142g/mol |
| 0.1mol |
| 0.5L |
(2)溶液是均匀的,取出10mL溶液的浓度与原溶液浓度相等为0.2mol/L;含有溶质质量为原溶液中的
| 1 |
| 50 |
| 1 |
| 50 |
(3)根据稀释定律,稀释后Na+的物质的量浓度=
| 0.2mol/L×2×0.01L |
| 0.1L |
| 0.002mol |
| 0.1mol/L |
Ⅱ.密度为1.04g/mL、36%的醋酸(CH3COOH)的物质的量浓度=
| 1000×1.04×36% |
| 60 |
| 0.25L×0.1mol/L |
| 6.24mol/L |
稀释浓溶液配制稀溶液,需要仪器有:10mL量筒,玻璃棒,250mL容量瓶,胶头滴管;
定容时仰视,液面在刻度线上方,所配溶液体积偏大,结合c=
| n |
| V |
故答案为:4.0;10mL量筒;玻璃棒;250mL容量瓶;胶头滴管;偏小.
点评:本题考查物质的量浓度计算、溶液配制,难度中等,注意根据物质的量浓度与质量分数之间的关系,根据c=
理解溶液配制原理与误差分析.
| n |
| V |

练习册系列答案
相关题目
已知有如下反应:Cl2+2I-=2Cl-+I2;Cl2+2Fe2+=2Cl-+2Fe3+;2Fe3++2I-=I2+2Fe2+;I2+SO2+2H2O=2I-+SO42-+4H+,下列叙述正确的是( )
| A、该反应是不可能发生的:Cl2+SO2+2H2O=2Cl-+SO42-+4H+ |
| B、氧化性:Cl2>Fe3+>I2 |
| C、还原性:I->Cl->Fe2+ |
| D、将SO2通入FeCl3溶液中得不到 SO42- |
 )为基本原料,经过反应得到一系列的芳炔类大环化合物,其结构为:
)为基本原料,经过反应得到一系列的芳炔类大环化合物,其结构为:
 )为起始物质,通过加成、消去反应制得.写出由苯乙烯制取苯乙炔的化学方程式(所需的无机试剂自选)
)为起始物质,通过加成、消去反应制得.写出由苯乙烯制取苯乙炔的化学方程式(所需的无机试剂自选)
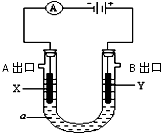 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板(X、Y都是惰性电极),A、B 是出口,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板(X、Y都是惰性电极),A、B 是出口,通过导线与直流电源相连.请回答以下问题: