题目内容
下列叙述中,正确的是( )
| A、核外电子排布完全相同的两种微粒的化学性质一定相同 |
| B、单原子形成的离子一定具有稀有气体原子的核外电子排布 |
| C、核外电子排布相同的两种原子一定属于同种元素 |
| D、所有主族元素的原子,形成单原子离子时的化合价和它的族序数相等 |
考点:原子核外电子排布,元素周期表的结构及其应用
专题:原子组成与结构专题
分析:A、核外电子排布完全相同的两种微粒不一定属于同种元素,化学性质不一定相同;
B、副族元素的单原子形成的离子不一定具有稀有气体原子的核外电子排布;
C、原子的质子数等于核外电子数;
D、主族元素的最高正化合价等于其族序数.
B、副族元素的单原子形成的离子不一定具有稀有气体原子的核外电子排布;
C、原子的质子数等于核外电子数;
D、主族元素的最高正化合价等于其族序数.
解答:
解:A、核外电子排布完全相同的两种微粒不一定属于同种元素,化学性质不一定相同,如Na+与F-核外电子排布相同,但是二者化学性质不同,故A错误;
B、副族元素的单原子形成的离子不一定具有稀有气体原子的核外电子排布,如成Fe2+的核外电子排布式为1s22s22p63s23p63d6,不具有稀有气体原子的核外电子排布,故B错误;
C、原子的质子数等于核外电子数,则核外电子排布相同的两种原子的质子数相同,一定属于同种元素,故C正确;
D、主族元素的最高正化合价等于其族序数,但是主族元素的原子,形成单原子离子时的化合价和它的族序数不一定相等,如Cl-的化合价为-1价,其族序数为7,故D错误;
故选C.
B、副族元素的单原子形成的离子不一定具有稀有气体原子的核外电子排布,如成Fe2+的核外电子排布式为1s22s22p63s23p63d6,不具有稀有气体原子的核外电子排布,故B错误;
C、原子的质子数等于核外电子数,则核外电子排布相同的两种原子的质子数相同,一定属于同种元素,故C正确;
D、主族元素的最高正化合价等于其族序数,但是主族元素的原子,形成单原子离子时的化合价和它的族序数不一定相等,如Cl-的化合价为-1价,其族序数为7,故D错误;
故选C.
点评:本题考查了原子结构、主族族序数与化合价的关系等,侧重于基础知识的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列方法不能用于金属防腐蚀处理的是( )
| A、涂防锈油漆 |
| B、将被保护的金属连接外加直流电源的正极 |
| C、电镀金属保护层 |
| D、与其它金属制成合金,如不锈钢 |
下列有关科学家的说法错误的是( )
| A、瑞典化学家舍勒命名了氯元素 |
| B、英国物理学家卢瑟福提出了带核的原子结构模型 |
| C、汤姆生发现电子打破了原子是不可分割的说法 |
| D、德国化学家维勒揭开了人工合成有机物的序幕 |
在密闭容器中发生下列反应2A(g)?cC(?)+2D(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述不正确的是( )
| A、C为非气态 |
| B、平衡向逆反应方向移动 |
| C、D的体积分数变小 |
| D、A的转化率变小 |
将10.6gNa2CO3和8.4gNaHCO3的混合物溶于水配成1L溶液,关于该溶液的说法错误的是( )
| A、溶液中:C(HCO3-)>C(CO32-) |
| B、溶液中:C(Na+)+C(H+)=2C(CO32-)+C(HCO3-)+C(OH-) |
| C、溶液中:2C(H+)+C(HCO3-)+3C(H2CO3)=C(CO32-)+2C(OH-) |
| D、该溶液的碱性强于0.1mol/L的Na2CO3溶液的碱性 |
元素符号、反应方程式、结构示意图、电子式、结构式等通常叫做化学用语.下列有关化学用语的表示方法中错误的是( )
A、异丁烷的结构式: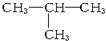 | ||
B、S2-的结构示意图: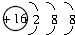 | ||
C、O-18的原子符号:
| ||
| D、CO2分子的结构式:O=C=O |
下列各组中的两种物质相互反应时,若改变反应条件(包括温度、反应物浓度、反应物用量比等),化学反应原理不改变的是( )
| A、Na和O2 |
| B、NaOH和CO2 |
| C、NaHCO3与盐酸 |
| D、MnO2与盐酸 |
下列所得溶液的物质的量浓度等于0.1mo/L的是( )
| A、将0.1mol氨气充分溶解在1L水中 |
| B、将10g质量分数为98%的硫酸与990g水混合 |
| C、将8g三氧化硫溶于水并配成1L溶液 |
| D、将0.1mol氧化钾溶于水并配成1L溶液 |