题目内容
m g H2O2与V L(标准状况)CO中所含氧原子数目相同,则m的数值是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:物质的量的相关计算
专题:计算题
分析:标准状况下,VL CO的物质的量是
mol,含有的氧原子的物质的量也是
mol,因此双氧水的物质的量是
mol,然后根据m=nM计算.
| V |
| 22.4 |
| V |
| 22.4 |
| V |
| 44.8 |
解答:
解:标准状况下,VL CO的物质的量是
=
mol,含有的氧原子的物质的量也是
mol.
根据二者所含氧原子数目相同可知双氧水的物质的量是
mol,根据m=nM可得:m=
mol×34g/mol=
g,
故选A.
| VL |
| 22.4mol/L |
| V |
| 22.4 |
| V |
| 22.4 |
根据二者所含氧原子数目相同可知双氧水的物质的量是
| V |
| 44.8 |
| V |
| 44.8 |
| 17V |
| 22.4 |
故选A.
点评:本题考查了物质的量的有关计算,难度不大,注意公式的联合应用和微粒种类.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
下列有关“焰色反应”说法中正确的是( )
| A、非金属单质燃烧时火焰均为无色 |
| B、所有金属及其化合物灼烧时火焰均有颜色 |
| C、NaCl与Na2CO3灼烧时火焰颜色相同 |
| D、焰色反应均应透过蓝色钴玻璃观察 |
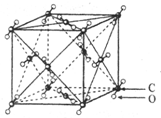 如图为干冰及其晶体的结构模型,下列有关分析正确的是( )
如图为干冰及其晶体的结构模型,下列有关分析正确的是( )| A、构成干冰的微粒是C原子和O原子 |
| B、CO2为极性分子 |
| C、干冰溶于水时有共价键要生成 |
| D、干冰中只存在微弱的分子间作用力 |
瓦斯中甲烷与氧气的质量比为1:4极易爆炸,此时氧气和甲烷的体积比为( )
| A、1:4 | B、1:2 |
| C、1:1 | D、2:1 |
A、B、C、D、E、F为六种短周期元素,它们的原子序数依次增大,A、D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C的最外层电子数相等,A与C形成的化合物常温下为液态.下列说法正确的是( )
| A、原子半径:D>E>F>C>B>A |
| B、A、C、D三种元素形成的化合物与C、D、F三种元素形成的化合物晶体类型相同,水溶液的酸碱性相同,造成溶液酸碱性的原理也相同 |
| C、A、C、E三种元素形成的化合物,在加热条件下一定能与铜反应 |
| D、B与F两种元素形成的一种化合物分子,各原子均达8电子结构,其中B显负价,F显正价,则该化合物与水反应生成ACF与BA3两种产物 |
 有机物A的结构如图所示,下列说法正确的是( )
有机物A的结构如图所示,下列说法正确的是( )| A、A能与碳酸氢钠溶液反应 |
| B、一定条件下,1mol A 能和5mol氢气发生加成反应 |
| C、一定条件下和浓溴水反应时,1mol A 能消耗 3mol Br2 |
| D、一定条件下,1mol A 能与3mol NaOH反应 |
实验室从海带中提取碘的操作过程中,仪器选用不正确的是( )
| 选项 | 操作 | 选用仪器 |
| A | 称取3g左右的干海带 | 托盘天平 |
| B | 灼烧干海带至完全变成灰烬 | 烧杯 |
| C | 过滤煮沸后的海带灰与水的混合液 | 漏斗 |
| D | 用四氯化碳从氧化后的海带灰浸取液中提取碘 | 分液漏斗 |
| A、A | B、B | C、C | D、D |
在标准状况下①2.24L CH4 ②3.01×1023个HCl分子 ③0.2mol NH3,下列对这四种气体的关系从大到小表达不正确的是( )
| A、体积②>③>① |
| B、物质的量 ②>③>① |
| C、质量③>②>① |
| D、氢原子个数③>②>① |
在下列溶液中,c(Cl-)与150mL 1mol/LAlCl3溶液中的c(Cl-)相等的是( )
| A、150mL 3mol/L的CaCl2溶液 |
| B、75mL 1.5mol/L的MgCl2溶液 |
| C、50mL 1 mol/L的FeCl2溶液 |
| D、225mL 2mol/L的NH4Cl溶液 |