题目内容
【题目】(1)单质钠是一种______色的金属,密度比水______![]() 大
大![]() 小
小![]() ,钠在自然界中以______
,钠在自然界中以______![]() 化合
化合![]() 游离
游离![]() 态存在;金属钠与水反应的化学方程式:______,金属钠在空气中燃烧生成______色的______
态存在;金属钠与水反应的化学方程式:______,金属钠在空气中燃烧生成______色的______![]() 化学式
化学式![]() ,其生成物与水反应的化学方程式:______。
,其生成物与水反应的化学方程式:______。
(2)氯气是一种______色的气体,密度比空气______,______溶于水,并可以和水发生反应,写出其反应的化学方程式:______,实验室中用______溶液![]() 化学式
化学式![]() 吸收多余的氯气。
吸收多余的氯气。
铁丝在氯气中燃烧的化学方程式:______。漂白粉是______和______![]() 化学式
化学式![]() 的混合物,是利用氯气与氢氧化钙反应制成的,写出其反应的方程式:______。
的混合物,是利用氯气与氢氧化钙反应制成的,写出其反应的方程式:______。
(3)现有物质:①氧化镁②硫酸铜③碳酸钙④金属钠⑤氯气⑥氢气⑦硫酸⑧氯水⑨二氧化硫⑩氧化钠![]() 二氧化硅
二氧化硅![]() 次氯酸
次氯酸![]() 漂白粉
漂白粉
按下列标准进行归类![]() 填序号
填序号![]() 混合物______酸______盐______单质______碱性氧化物______酸性氧化物______。
混合物______酸______盐______单质______碱性氧化物______酸性氧化物______。
【答案】银白 小 化合 ![]() 淡黄
淡黄 ![]()
![]() 黄绿 大 易
黄绿 大 易 ![]() NaOH
NaOH 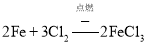
![]()
![]()
![]() ⑧
⑧![]() ⑦
⑦![]() ②③ ④⑤⑥ ①
②③ ④⑤⑥ ①![]() ⑨
⑨![]()
【解析】
![]() 钠观察切开面,新切开的金属钠断面呈银白色色;密度比水小,钠是很活泼的金属,在自然界中只能以化合态存在;金属钠与水反应生成氢氧化钠和氢气;
钠观察切开面,新切开的金属钠断面呈银白色色;密度比水小,钠是很活泼的金属,在自然界中只能以化合态存在;金属钠与水反应生成氢氧化钠和氢气;
金属钠在空气中燃烧生成淡黄色的过氧化钠,过氧化钠可以和水之间发生反应生成氢氧化钠和氧气;
![]() 在通常状况下,氯气是一种黄绿色气体,密度比空气大,易溶于水;氯气和水反应生成盐酸和次氯酸,实验室用氢氧化钠吸收吸收多余的氯气,铁丝在氯气中燃烧生成氯化铁,氯气与氢氧化钙反应生成漂白粉,漂白粉的主要成分是次氯酸钙、氯化钙;
在通常状况下,氯气是一种黄绿色气体,密度比空气大,易溶于水;氯气和水反应生成盐酸和次氯酸,实验室用氢氧化钠吸收吸收多余的氯气,铁丝在氯气中燃烧生成氯化铁,氯气与氢氧化钙反应生成漂白粉,漂白粉的主要成分是次氯酸钙、氯化钙;
![]() 物质分为混合物和纯净物,纯净物又分为单质和化合物,化合物分为氧化物、酸、碱、盐。混合物是指由多种物质组成的物质;酸是指电离时产生的阳离子全部是氢离子的化合物;盐是指由金属离子和酸根离子组成的化合物;单质是只含有一种元素的纯净物;氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素,碱性氧化物是指能和酸反应生成盐和水的氧化物,酸性氧化物是指能和碱反应生成盐和水的氧化物。
物质分为混合物和纯净物,纯净物又分为单质和化合物,化合物分为氧化物、酸、碱、盐。混合物是指由多种物质组成的物质;酸是指电离时产生的阳离子全部是氢离子的化合物;盐是指由金属离子和酸根离子组成的化合物;单质是只含有一种元素的纯净物;氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素,碱性氧化物是指能和酸反应生成盐和水的氧化物,酸性氧化物是指能和碱反应生成盐和水的氧化物。
![]() 钠观察切开面,新切开的金属钠断面呈银白色色;钠与水反应浮在水面上,钠的密度比水小,钠是很活泼的金属,在常温下就能与氧气反应,钠在自然界中只能以化合态存在;金属钠与水反应生成氢氧化钠和氢气,反应的化学方程式:
钠观察切开面,新切开的金属钠断面呈银白色色;钠与水反应浮在水面上,钠的密度比水小,钠是很活泼的金属,在常温下就能与氧气反应,钠在自然界中只能以化合态存在;金属钠与水反应生成氢氧化钠和氢气,反应的化学方程式:![]() ,金属钠在空气中燃烧生成淡黄色的过氧化钠,
,金属钠在空气中燃烧生成淡黄色的过氧化钠,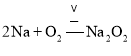 ,过氧化钠可以和水之间发生反应生成氢氧化钠和氧气,方程式为:
,过氧化钠可以和水之间发生反应生成氢氧化钠和氧气,方程式为:![]() ;
;
![]() 在通常状况下,氯气是一种黄绿色气体,密度比空气大,易溶于水,1体积水中能溶解2体积的氯气;氯气和水反应生成盐酸和次氯酸,
在通常状况下,氯气是一种黄绿色气体,密度比空气大,易溶于水,1体积水中能溶解2体积的氯气;氯气和水反应生成盐酸和次氯酸,![]() ,实验室用氢氧化钠吸收吸收多余的氯气,生成氯化钠和次氯酸钠,离子反应为
,实验室用氢氧化钠吸收吸收多余的氯气,生成氯化钠和次氯酸钠,离子反应为![]() ,铁丝在氯气中燃烧生成氯化铁
,铁丝在氯气中燃烧生成氯化铁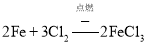 ,氯气与石灰乳反应生成氯化钙和次氯酸钙,反应的方程式为
,氯气与石灰乳反应生成氯化钙和次氯酸钙,反应的方程式为![]() ,漂白粉的主要成分是次氯酸钙
,漂白粉的主要成分是次氯酸钙![]() 、氯化钙
、氯化钙![]() ;漂白粉溶于水后,受空气中的
;漂白粉溶于水后,受空气中的![]() 作用,即产生有漂白、杀菌作用的次氯酸,同时生成碳酸钙沉淀,反应的化学方程式为:
作用,即产生有漂白、杀菌作用的次氯酸,同时生成碳酸钙沉淀,反应的化学方程式为:![]() ;
;
![]() 氧化镁为碱性氧化物;
氧化镁为碱性氧化物;![]() 硫酸铜由硫酸根离子和铜离子构成的盐;
硫酸铜由硫酸根离子和铜离子构成的盐;![]() 碳酸钙由碳酸根离子和钙离子构成的盐;
碳酸钙由碳酸根离子和钙离子构成的盐;![]() 金属钠属于单质;
金属钠属于单质;![]() 氯气属于单质;
氯气属于单质;![]() 氢气属于单质;
氢气属于单质;![]() 硫酸属于二元强酸;
硫酸属于二元强酸;![]() 氯水属于氯气和水的混合物;
氯水属于氯气和水的混合物;![]() 二氧化硫为酸性氧化物;
二氧化硫为酸性氧化物;![]() 氧化钠为碱性氧化物;
氧化钠为碱性氧化物;![]() 二氧化硅为酸性氧化物;
二氧化硅为酸性氧化物;![]() 次氯酸为一元弱酸;
次氯酸为一元弱酸;![]() 漂白粉主要成分是次氯酸钙
漂白粉主要成分是次氯酸钙![]() 、氯化钙
、氯化钙![]() ,属于混合物;
,属于混合物;
则:混合物为![]() ,酸为
,酸为![]() ,盐为
,盐为![]() ,单质为
,单质为![]() ,碱性氧化物为
,碱性氧化物为![]() ,酸性氧化物为
,酸性氧化物为![]() 。
。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案