题目内容
11.A、B、C、D、E为五种常见的短周期元素,常温下,A、B可形成B2A2和B2A两种液态化合物,B与D可组成气态分子X,X的水溶液呈碱性,C元素的焰色反应呈黄色,E与C同周期,且E的最高价氧化物对应的水化物呈两性.试回答:(1)写出X的电子式
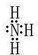 ;
;(2)由A、C、E三种元素形成的盐的水溶液呈碱性,用离子方程式解释其原因AlO2-+2H2O=Al(OH)3+OH-;
(3)A、B、D按3:4:2组成的化合物是离子化合物.(填“离子”或“共价”)
(4)用A单质和B单质可制取气体燃料电池,该电池用多孔的惰性电极浸入浓KOH溶液,两极分别通入A单质和B单质.写出该电池负极的电极反应式:H2-2e-+2OH-=2H2O.
分析 A、B、C、D、E为五种常见的短周期元素,常温下,A、B可形成B2A2和B2A两种液态化合物,则B为H,A为O;B与D可组成气态分子X,X的水溶液呈碱性,可知D为N,X为NH3;C元素的焰色反应呈黄色,E与C同周期,且E的最高价氧化物对应的水化物呈两性,可知C为Na、E为Al,以此来解答.
解答 解:A、B、C、D、E为五种常见的短周期元素,常温下,A、B可形成B2A2和B2A两种液态化合物,则B为H,A为O;B与D可组成气态分子X,X的水溶液呈碱性,可知D为N,X为NH3;C元素的焰色反应呈黄色,E与C同周期,且E的最高价氧化物对应的水化物呈两性,可知C为Na、E为Al,
(1)X的电子式为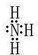 ,故答案为:
,故答案为: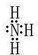 ;
;
(2)由A、C、E三种元素形成的盐为NaAlO2,水溶液呈碱性,发生水解离子反应为AlO2-+2H2O=Al(OH)3+OH-,
故答案为:AlO2-+2H2O=Al(OH)3+OH-;
(3)A、B、D按3:4:2组成的化合物为NH4NO3,含离子键,是离子化合物,故答案为:离子;
(4)氢气、氧气、KOH构成的原电池中,氢气在负极上失去电子,则负极反应为H2-2e-+2OH-=2H2O,故答案为:H2-2e-+2OH-=2H2O.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素化合物知识推断元素为解答的关键,侧重分析与应用能力的考查,注意盐类水解、电极反应的应用,题目难度不大.

练习册系列答案
相关题目
7.下列离子方程式的书写正确的是( )
| A. | 漂白粉溶液中通入SO2气体 Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| B. | 碳酸氢钙溶液中加入过量的氢氧化钠溶液 HCO3-+OH-═CO32-+H2O | |
| C. | 明矾溶液中加入过量的Ba(OH)2溶液2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ | |
| D. | 过量的NH4HSO4溶液与Ba(OH)2溶液反应2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
19.下列清洗方法错误的是( )
| A. | 用肥皂洗涤久置石灰水的试剂瓶 | B. | 用酒精清洗残留碘的试管 | ||
| C. | 用洗涤剂清洗餐具上的油污 | D. | 用汽油清洗沾在手上的油漆 |
6.下列热化学方程式中,正确的是( )
| A. | 甲烷的标准燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ 其热化学方程式为:N2(g)+3H2(g)$?_{500℃/30MPa}^{催化剂}$2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则1mol稀H2SO4和足量KOH反应的反应热为△H=2×(-57.3)kJ/mol | |
| D. | 同温同压下H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件的△H不同 |
16.下列各种说法中,都包含有前后两个数值,其中前者大于后者的是( )
| A. | 在25℃和80℃时纯水中的c(H+)浓度 | |
| B. | 室温时,浓度均为 0.1mol/L的(NH4)2SO4(aq)、(NH4)2CO3 (aq)的c(NH4+) | |
| C. | 25℃时,pH均为3的HCl和NH4Cl溶液中水的电离程度 | |
| D. | 1 L饱和氯化铵溶液中NH4+ 和Cl- 的个数 |
3.以下物质中,能与Na,NaOH,NaHCO3,都反应的物质是( )
| A. | 乙醇 | B. | 乙酸 | C. | 乙烷 | D. | 乙烯 |
1.向100mL沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热.下列有关分析正确的是( )
| A. | 所得液体属于纯净物 | B. | 该红褐色液体能产生了达尔效应 | ||
| C. | 所得液体中分散质粒子只有Fe(OH)3 | D. | 上述实验过程中没有发生化学变化 |
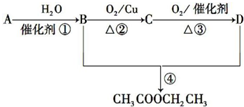 已知:①A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工发展水平;②2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
已知:①A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工发展水平;②2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.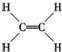 .
. 元素在周期表中的位置,反映了元素的原子结构和元素性质.如图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素性质.如图是元素周期表的一部分.