题目内容
9.一定条件下,通过下列反应可实现汽车尾气的合理排放:2NO(g)+2CO(g)$\stackrel{催化剂}{?}$N2(g)+2CO2(g)△H<0,若反应在恒容的密闭容器中进行,下列说法正确的是( )| A. | 随着反应的进行,容器内压强始终不变 | |
| B. | 及时地分离出N2或CO2,正反应速率加快 | |
| C. | 升高温度(其它条件不变),可提高反应物的转化率 | |
| D. | 使用不同催化剂(其它条件不变),该反应的平衡常数不变 |
分析 A.反应前后气体体积减小,气体压强之比等于气体物质的量之比分析;
B.及时地分离出N2或CO2,生成物浓度减小,反应速率减小;
C.反应是放热反应,升温平衡逆向进行;
D.催化剂改变反应速率不改变化学平衡,平衡常数随温度变化.
解答 解:A.反应前后气体体积减小,气体压强之比等于气体物质的量之比,随着反应的进行,容器内压强始终改变,达到平衡状态,气体压强不变,故A错误;
B.及时地分离出N2或CO2,生成物浓度减小,反应速率减小,正逆反应速率减小,故B错误;
C.反应是放热反应,升温平衡逆向进行,反应物的转化率减小,故C错误;
D.催化剂改变反应速率不改变化学平衡,平衡常数随温度变化,使用不同催化剂(其它条件不变),该反应的平衡常数不变,故D正确;
故选D.
点评 本题考查了化学平衡影响因素分析判断,主要是物质浓度、气体压强、温度对化学平衡影响的理解应用,化学平衡移动原理是解题关键,题目较简单.

练习册系列答案
相关题目
19.下列离子方程式错误的是( )
| A. | 证明醋酸的酸性比碳酸强:2CH3COOH+CaCO3═Ca2++H2O+2CH3COO-+CO2↑ | |
| B. | 证明FeCl2溶液已变质:Fe3++3SCN-═Fe(SCN)3 | |
| C. | 证明Al(OH)3有酸性:Al( OH)3+NH3•H2O═AlO2-+NH4++2H2O | |
| D. | 证明氧化性Fe3+>Cu2+:2Fe3++Cu═Cu2++2Fe2+ |
20.室温下,下列各组离子能大量共存的是( )
| A. | 通入大量CO2的溶液中:K+、ClO-、SO32-、HCO3- | |
| B. | 能使蓝色石蕊试纸变红色的溶液中:K+、Na+、CO32-、NO3- | |
| C. | 含有较多Al3+的溶液:Na+、SO42-、I-、ClO- | |
| D. | c(H+):c(OH-)=1:1012的水溶液中:CO32-、Na+、NO3-、AlO2- |
17.下列关于物质的分离表述不正确的是( )
| A. | 用蒸馏法可实现海水的淡化 | |
| B. | 乙醇可以用作“提取碘水中的碘”的萃取剂 | |
| C. | 用“蒸发结晶”的方法从氯化钠溶液中分离得到氯化钠晶体 | |
| D. | 除去氧化铁中的氧化铝杂质:用NaOH溶液浸泡,再过滤、洗涤、干燥,即可得到纯净氧化铁 |
4.下列关于Al及其化合物的性质描述正确的是( )
| A. | 金属铝能够在空气中稳定存在是因为其在常温下不与氧气反应 | |
| B. | 氧化铝与NaOH溶液的反应体现了氧化铝的酸性氧化物的特性 | |
| C. | 明矾的水溶液具有“净水、杀菌消毒”的作用 | |
| D. | 氢氧化铝是两性氢氧化物,其“两性”是指既具有氧化性,又具有还原性 |
1.离子晶体熔点的高低决定于阴、阳离子核间距离、离子电荷数和晶格能的大小,据所学知识判断KCl、NaCl、CaO、BaO四种晶体熔点的高低顺序是( )
| A. | KCl>NaCl>BaO>CaO | B. | NaCl>KCl>CaO>BaO | ||
| C. | CaO>BaO>NaCl>KCl | D. | CaO>BaO>KCl>NaCl |
18.有A、B、C、D四种物质,已知它们能发生如下反应:
①A2++B═B2++A ②A2++C═C2++A
③B2++C═C2++B ④C2++D═D2++C( )
①A2++B═B2++A ②A2++C═C2++A
③B2++C═C2++B ④C2++D═D2++C( )
| A. | 氧化性:A2+>B2+>C2+>D2+ | B. | 氧化性:D2+>C2+>B2+>A2+ | ||
| C. | 还原性:A>B>C>D | D. | 还原性:C>D>B>A |
19.下列有关说法错误的是( )
| A. | 物质在不电离的条件下,也能导电 | |
| B. | 若化学平衡向逆反应方向移动,则正反应速率不一定减小 | |
| C. | 硫酸钡、醋酸铵、碳酸氢钠都是强电解质 | |
| D. | 导电性强的溶液里自由移动离子数目一定比导电性弱的溶液里自由移动离子数目多 |
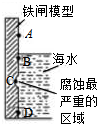 铁及其化合物与生产、生活关系密切,
铁及其化合物与生产、生活关系密切,