题目内容
6. 现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题:
现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题:(1)写出C、D、E三种原子第一电离能由大到小的顺序为F>N>O.(用元素符号表示)
(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为H2O>NH3>CH4(用分子式表示),根据价层电子对互斥理论预测BA2D的分子构型为平面三角形.
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据六面体互不相邻的顶点,而六面体的每条棱上均有一个BC-.与A同族且相隔两个周期的元素R的离子位于立方体的恰当位置上.根据其结构特点可知该晶体的化学式为(用最简正整数表示)KFe2(CN)6.
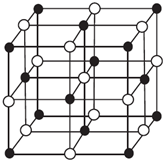
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是Cr2O3.
分析 B的s能级上电子总数等于p能级上电子总数的2倍,B的电子排布是1s22s22p2,则B是碳元素;结合B、C、D、E、A五种非金属元素原子半径依次减小,根据元素周期律知元素分别是碳、氮、氧、氟、氢,即A为H、C为N、D为O、E为F.X原子的M能层上有4个未成对电子,则其价电子排布式是3d64s2,则X是Fe.
(1)同周期主族元素,从左到右元素的第一电离能呈增大趋势,但是氮原子的2p轨道上电子半充满,较稳定,第一电离能比氧的大;
(2)元素的电负性越强,气态氢化物就越稳定;根据价层电子对互斥理论计算甲醛HCHO中C原子价层电子对数,确定空间结构;
(3)与A同族且相隔两个周期的元素R为K元素,根据均摊法,铁原子有8×$\frac{1}{8}$=1,Fe2+、Fe3+离子各占一半,总电荷为+2.5,CN-为12×$\frac{1}{4}$=3,所带电荷为-3,根据电中性知K+应是0.5个;
(4)对于离子晶体,晶格能越大,熔点越高;MgO与NaCl晶胞结构相似,以图中体心白色球为Mg2+,则黑色球为O2-;
(5)V的价电子排布式是3d34s2,有3对孤对电子,Cr的价电子排布式是3d54s1,有5对孤对电子.
解答 解:B的s能级上电子总数等于p能级上电子总数的2倍,B的电子排布是1s22s22p2,则B是碳元素;结合B、C、D、E、A五种非金属元素原子半径依次减小,根据元素周期律知元素分别是碳、氮、氧、氟、氢,即A为H、C为N、D为O、E为F.X原子的M能层上有4个未成对电子,则其价电子排布式是3d64s2,则X是Fe.
(1)同周期主族元素,从左到右元素的第一电离能呈增大趋势,但是氮原子的2p轨道上电子半充满,较稳定,第一电离能比氧的大,故第一电离能:F>N>O,
故答案为:F>N>O;
(2)元素的电负性越强,气态氢化物就越稳定,非金属性O>N>C,氢化物稳定性由强到弱的顺序为:H2O>NH3>CH4,
根据价层电子对互斥理论,CH2O的中心原子的杂化方式为sp2杂化,为平面三角形,
故答案为:H2O>NH3>CH4;平面三角形;
(3)与A同族且相隔两个周期的元素R为K元素,由题目信息,根据均摊法,晶胞中铁原子有8×$\frac{1}{8}$=1,Fe2+、Fe3+离子各占一半,总电荷为+2.5,CN-为12×$\frac{1}{4}$=3,所带电荷为-3,根据电中性知K+应是0.5个,故化学式为:KFe2(CN)6,
故答案为:KFe2(CN)6;
(4)对于离子晶体,晶格能越大,熔点越高,则熔沸点TiN>MgO>KCl,MgO与NaCl晶胞结构相似,以图中体心白色球为Mg2+,则黑色球为O2-,1个Mg2+周围和它最邻近且等距离的O2-有6个,
故答案为:TiN>MgO>KCl;6;
(5)V的价电子排布式是3d34s2,有3对孤对电子,Cr的价电子排布式是3d54s1,有5对孤对电子,Cr2O3含未成对电子多,则磁性大,磁记录性能越好,
故答案为:Cr2O3.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、元素周期律、电离能、晶胞结构、晶体类型与性质等,注意理解同周期第一电离能异常情况,(3)中注意利用电荷守恒确定钾离子数目.

 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案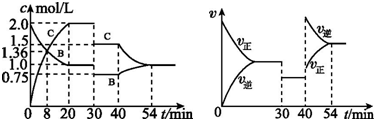
下列说法中正确的是( )
| A. | 30 min~40 min 间该反应使用了催化剂 | |
| B. | 反应方程式中的x=2,正反应为吸热反应 | |
| C. | 30 min 时条件的变化是降低压强,40 min 时条件的变化是升高温度 | |
| D. | 前8 min A 的平均反应速率为0.08 mol•L-1•min-1 |

| A. | 苯氧乙酸甲酯的分子式为C9H10O3 | |
| B. | 苯氧乙酸与邻羟基苯乙酸不互为同分异构体 | |
| C. | 苯酚和邻羟基苯乙酸可用FeCl3溶液检验 | |
| D. | ClCH2COOH与足量烧碱溶液共热所得有机物为HOCH2COOH |
| A. | 每摩尔花生四烯酸最多可与4 mol溴发生加成反应 | |
| B. | 它可以使酸性高锰酸钾溶液褪色 | |
| C. | 它可与乙醇发生酯化反应 | |
| D. | 它是食醋的主要成分 |
| A. | c(SO3)=0.4 mol/L | B. | c(SO2)=c(SO3)=0.15 mol/L | ||
| C. | c(O2)=0.35 mol/L | D. | c(SO2)+c(SO3)=0.4 mol/L |
制备苯乙烯(原理如图所示):
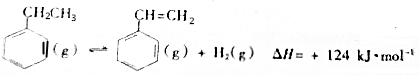
(1)部分化学键的键能如下表:
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•molˉ1 | 412 | 348 | x | 436 |
(2)工业上,在恒压设备中进行反应时,常在乙苯蒸气中通入一定量的水蒸气,用化学平衡理论解释通入水蒸气的原因为正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动,提高乙苯的平衡转化率..
| A. | 稀盐酸可除去烧瓶内残留的MnO2 | B. | 可用无色广口玻璃瓶保存氨水 | ||
| C. | 稀硝酸可除去试管内壁粘有的硫磺 | D. | 煮沸自来水可除去其中的Ca(HCO3)2 |
| A | 向盐酸酸化的Ba(NO3)2溶液中通入SO2 | 有白色沉淀生成 | BaSO3难溶于酸 |
| B | 向等浓度的KCl、Kl混合液中滴加AgNO3溶液 | 先出现白色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 溴乙烷与NaOH水溶液共热后,加HNO3酸化,滴加AgNO3溶液 | 出现淡黄色沉淀 | 溴乙烷含溴元素 |
| D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| A. | A | B. | B | C. | C | D. | D |
 .
.