题目内容
 下列叙述正确的是( )
下列叙述正确的是( )| A、为提醒人们在使用浓H2SO4时要注意安全,贮存浓H2SO4的容器上贴有右图标识 |
| B、实验室可通过蒸馏的方法除去自来水中含有的Cl-等杂质制蒸馏水 |
| C、做焰色反应实验时,应先将铂丝(或铁丝)用稀硫酸洗净后,在酒精灯外焰上灼烧至没有颜色时,再蘸取待检溶液进行实验 |
| D、由于碱金属单质化学性质活泼,实验室中的各种碱金属单质均保存在煤油中 |
考点:化学试剂的分类,焰色反应,化学试剂的存放,物质的分离、提纯和除杂
专题:实验评价题
分析:A.浓H2SO4有腐蚀性;
B.自来水加热蒸发,冷却后可得蒸馏水;
C.铂丝用用稀盐酸洗净;
D.锂比煤油的密度小.
B.自来水加热蒸发,冷却后可得蒸馏水;
C.铂丝用用稀盐酸洗净;
D.锂比煤油的密度小.
解答:
解:A.浓H2SO4有腐蚀性,是腐蚀品,不是剧毒品,故A错误;
B.自来水中含有的Cl-等杂质,蒸馏时,可将水和杂质分离,可得到纯净的水,故B正确;
C.铂丝用用稀盐酸洗净,不能用稀硫酸,硫酸盐难挥发,故C错误;
D.碱金属中锂比煤油的密度小,应用石蜡密封,故D错误.
故选B.
B.自来水中含有的Cl-等杂质,蒸馏时,可将水和杂质分离,可得到纯净的水,故B正确;
C.铂丝用用稀盐酸洗净,不能用稀硫酸,硫酸盐难挥发,故C错误;
D.碱金属中锂比煤油的密度小,应用石蜡密封,故D错误.
故选B.
点评:本题考查物质的分类、提纯、检验和保存,明确物质的性质与保存方法的关系是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
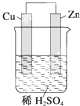 如图是Zn和Cu形成的原电池,则下列结论中正确的是( )
如图是Zn和Cu形成的原电池,则下列结论中正确的是( )①铜为阳极,锌为阴极;②铜极上有气泡;③SO
2- 4 |
| A、①②③ | B、②④⑥ |
| C、②③⑥ | D、③④⑤ |
下列离子方程式不正确的是( )
| A、将一小粒金属钠加入水中:2Na+2H2O=2Na++2OH-+H2↑ |
| B、硅酸钠溶液中滴加稀盐酸:SiO32-+2H+═H2SiO3↓ |
| C、向CuSO4溶液中加入适量Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ |
| D、澄清石灰水中通入过量的二氧化碳:OH-+CO2═HCO3- |
1,8-二硝基萘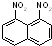 苯环上的二溴代物与四溴代物的种类分别有( )
苯环上的二溴代物与四溴代物的种类分别有( )
 苯环上的二溴代物与四溴代物的种类分别有( )
苯环上的二溴代物与四溴代物的种类分别有( )| A、9种、9种 |
| B、9种、15种 |
| C、15种、9种 |
| D、15种、15种 |
原计划实现全球卫星通讯需发射77颗卫星,这与铱(Ir〕元素的原子核外电子数恰好相等,因此称为“铱星计划”.已知铱的一种同位素是
Ir,则其核内的质量数是( )
191 77 |
| A、77 | B、286 |
| C、191 | D、114 |
一个氖原子的质量是a g,一个12C原子的质量为b g,NA表示阿伏德罗常数,下列说法不正确的是( )
A、该氖原子的相对原子质量是
| ||
| B、氖原子的摩尔质量为a?NA g/mol | ||
C、Wg该氖原子的物质的量为
| ||
D、Wg该氖原子所含原子数为
|
下列有关热化学方程式的叙述正确的是( )
| A、已知CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-893.0kJ/mol,则甲烷的燃烧热为893.0kJ?mol-1 | ||
| B、已知4P(红磷,s)═P4(白磷,s);△H>0,则白磷比红磷稳定 | ||
C、含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,反应的化学方程式为:NaOH(aq)+
| ||
D、己知C(s)+O2(g)═CO2(g);△H1C(s)+
|
下列热化学方程式或离子方程式中,正确的是( )
| A、甲烷的燃烧热为890.3 kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ?mol-1 | ||||||||
| B、500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中完全反应生成NH3(g),放热19.3 kJ,其热化学方程式为: N2(g)+3H2(g)
| ||||||||
| C、氯化镁溶液与氨水反应:Mg 2++2OH -=Mg(OH)2↓ | ||||||||
D、已知强酸与强碱的稀溶液反应的中和热为57.3 KJ/mol,则0.1mol醋酸与0.1mol氢氧化钠的稀溶液反应的热化学方程式为:
|
下列有机物的命名正确的是( )
A、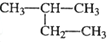 2-乙基丙烷 2-乙基丙烷 |
| B、CH3-CH=CH-CH3 2-丁烯 |
C、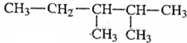 3,4─二甲基戊烷 3,4─二甲基戊烷 |
D、 二甲基苯 二甲基苯 |