题目内容
15.有8种物质:①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥溴乙烷;⑦聚丙烯;⑧环己烯.其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
分析 含碳碳双键、三键的有机物与溴水、高锰酸钾均反应,苯的同系物与高锰酸钾反应,以此来解答.
解答 解:②乙烯、③乙炔、⑧环己烯与溴水、高锰酸钾均反应;
⑤甲苯能使酸性KMnO4溶液褪色,
则只有①④⑥⑦既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪,
故选C.
点评 本题考查有机物的结构和性质,侧重于学生的分析能力的考查,为高考常见题型,注意把握有机物的结构和官能团的性质为解答该类题目的关键,题目难度不大.

练习册系列答案
相关题目
3.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 16 g O2中含有的氧分子数为NA | |
| B. | 1 mol Mg变为Mg2+时失去的电子数目为2NA | |
| C. | 常温常压下,11.2 L H2中含有的氢分子数为0.5NA | |
| D. | 1 mol•L-1 CaCl2溶液中含有的氯离子数为NA |
10.以下名称、化学用语均正确的是( )
| A. | 笨的实验式:CH | B. | 二氯乙稀的结构简式:CH2=C(Cl)2 | ||
| C. | 甲酸的结构式: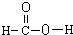 | D. | 醛基的电子式: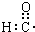 |
7.在体积固定,容积为2L的密闭容器中进行如下化学反应:
CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.
(2)该反应为吸热反应(填“吸热”或“放热”).
(3)能判断该反应一定达到化学平衡状态的依据是BC.
A.容器中压强不再改变 B.混合气体中c(CO)不再改变
C.v(H2)正=v(H2O)逆 D.c(CO2)=c(CO)
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为
2mol/L,c(H2)为1.5mol/L,c(CO)为1mol/L,c(H2O)为3mol/L,则下一时刻,反应向逆向(填“正向”或“逆向”)进行.
(5)保持容器体积不变,下列措施中一定能使H2的转化率增大的有CD.
A.充入氦气
B.使用催化剂
C.平衡后再向容器内通入一定量CO2
D.升高温度
(6)在830℃时,发生上述反应,若开始时加入0.3mol CO2和0.2mol H2,经过3分钟刚好达到平衡,以CO的浓度变化表示的化学反应速率为v(CO)=0.02mol•L-1•min-1.
CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.
(2)该反应为吸热反应(填“吸热”或“放热”).
(3)能判断该反应一定达到化学平衡状态的依据是BC.
A.容器中压强不再改变 B.混合气体中c(CO)不再改变
C.v(H2)正=v(H2O)逆 D.c(CO2)=c(CO)
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为
2mol/L,c(H2)为1.5mol/L,c(CO)为1mol/L,c(H2O)为3mol/L,则下一时刻,反应向逆向(填“正向”或“逆向”)进行.
(5)保持容器体积不变,下列措施中一定能使H2的转化率增大的有CD.
A.充入氦气
B.使用催化剂
C.平衡后再向容器内通入一定量CO2
D.升高温度
(6)在830℃时,发生上述反应,若开始时加入0.3mol CO2和0.2mol H2,经过3分钟刚好达到平衡,以CO的浓度变化表示的化学反应速率为v(CO)=0.02mol•L-1•min-1.
4.从香荚兰豆中提取的有机物A用来合成人工香料,其结构简式如图所示,下列关于物质A的说法正确的是( )
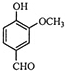

| A. | A的分子式是C8H10O3 | B. | A分子中含有酯基 | ||
| C. | A只能发生取代反应 | D. | A能与Na反应 |
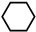 (g)$?_{高温}^{FeSO_{4}/Al_{2}O_{3}}$
(g)$?_{高温}^{FeSO_{4}/Al_{2}O_{3}}$ (g)+3H2(g)
(g)+3H2(g)