题目内容
18.下列有关化学用语的表述正确的是( )| A. | 质子数为35、中子数为45的溴原子:${\;}_{45}^{80}$Br | |
| B. | 丙烷分子的球棍模型为: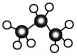 | |
| C. | 次氯酸的电子式为: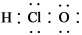 | |
| D. | -OH与OH-组成元素相同,含有的电子数也相同 |
分析 A.元素符号的左下角为质子数,不是中子数;
B.丙烷分子中含有两个甲基、1个亚甲基,碳原子半径大于氢原子;
C.次氯酸的中心原子为O原子,分子中不存在H-Cl键;
D.羟基为中性原子团,含有9个电子,而氢氧根离子含有10个电子.
解答 解:A.质子数为35、中子数为45的溴原子的质量数为80,该原子正确的表示方法为:3580Br,故A错误;
B.丙烷为含有3个碳原子的烷烃,丙烷分子的球棍模型为: ,故B正确;
,故B正确;
C.次氯酸分子中含有1个氢氧键和1个O-Cl键,其电子式为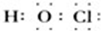 ,故C错误;
,故C错误;
D.-OH与OH-组成元素相同,二者含有的电子数分别为9、10,含有电子数不相同,故D错误;
故选B.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及电子式、球棍模型、元素符号等知识,明确常见化学用语的书写原则为解答结构,注意掌握甲基与甲烷、羟基与氢氧根离子的区别,为易错点.

练习册系列答案
相关题目
3.一定温度下,在1L密闭容器中,反应N2+3H2?2NH3达到化学平衡状态的标志是( )
| A. | N2:H2:NH3=1:3:2 | |
| B. | N2、H2、NH3的物质的量不再改变 | |
| C. | 混合气体的密度保持不变 | |
| D. | 单位时间里每增加1mol N2,同时增加3mol H2 |
10.下列化学用语正确的是( )
| A. | H2O2的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-H+ | |
| B. | 次氯酸的结构式:H-O-Cl | |
| C. | S2-的结构示意图: | |
| D. | CO2的比例模型: |
7.海洋约占地球表面的71%,具有十分巨大的开发潜力,目前的南海争端威胁到我们国家的核心利益.下列关于海水资源的说法中,错误的是( )
| A. | 海带中含有碘元素 | |
| B. | 海水中含有大量氯元素 | |
| C. | 蒸馏法是海水淡化的主要方法之一 | |
| D. | 开发海水资源可以不考虑是否对环境有污染 |
8.下列关于有机化合物的认识正确的是( )
| A. | 石油的分馏、煤的干馏都是属于物理变化 | |
| B. | 淀粉、纤维素、油脂、蛋白质都是天然有机高分子化合物 | |
| C. | 蛋白质溶液遇硫酸铵溶液和硫酸铜溶液后都产生的沉淀,且原理相同 | |
| D. | 植物油能使溴的四氯化碳溶液褪色 |
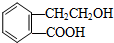 ,它可通过不同化学反应分别制得B、C、D和E四种物质
,它可通过不同化学反应分别制得B、C、D和E四种物质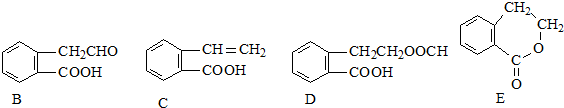
 ;A→D:
;A→D: .
. .
.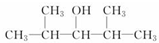 B.
B.
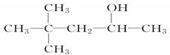 D.CH3(CH2)5CH2OH
D.CH3(CH2)5CH2OH