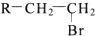题目内容
 在Na2O2与水反应实验中,发现Na2O2与水反应后的溶液中滴加酚酞试液溶液呈现红色,但红色很快褪色,甲、乙、丙三同学对此分别做了如下推测.
在Na2O2与水反应实验中,发现Na2O2与水反应后的溶液中滴加酚酞试液溶液呈现红色,但红色很快褪色,甲、乙、丙三同学对此分别做了如下推测.甲:因为反应后试管很热,所以可能是溶液温度较高使红色褪去.
乙:因为所加水的量较少,红色褪去可能是生成的NaOH溶液浓度较大的影响.
丙:Na2O2具有强氧化性,生成物中O2、H2O2(可能产物)等也具有强氧化性,可能氧化漂白了红色物质.
(1)验证甲同学的推测不正确的方法
(2)验证乙同学的推测不正确的方法
(3)当出现
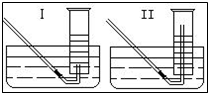
(4)有同学提出用定量的方法探究丙同学方案中是否含有H2O2.实验方法:称取2.6gNa2O2(M=78)固体,使之与足量的水反应,测量产生O2的体积,与理论值比较,即可得出结论.测量气体体积,必须待试管和量筒内的气体都冷却至室温时进行.则该实验选用如图
考点:性质实验方案的设计,实验装置综合
专题:实验设计题
分析:(1)甲同学的推测与温度有关;
(2)乙同学的推测,与碱的浓度有关;
(3)强氧化性氧化漂白了红色物质,为永久性漂白,改变温度、碱的浓度均不能恢复红色;
(4)称取2.6gNa2O2(M=78)固体,n(Na2O2)=
=0.033mol,由2Na2O2+2H2O=4NaOH+O2↑可知,生成氧气为0.033×
×22.4L/mol=0.3696L,选择量筒的规格与气体体积相近,且测量气体体积时,为防止倒吸应将导管尽量插入量筒底部,以此来解答.
(2)乙同学的推测,与碱的浓度有关;
(3)强氧化性氧化漂白了红色物质,为永久性漂白,改变温度、碱的浓度均不能恢复红色;
(4)称取2.6gNa2O2(M=78)固体,n(Na2O2)=
| 2.6g |
| 78g/mol |
| 1 |
| 2 |
解答:
解:(1)甲同学的推测与温度有关,则验证甲同学的推测不正确的方法为冷却后溶液不变红,故答案为:冷却后溶液不变红;
(2)乙同学的推测,与碱的浓度有关,则验证乙同学的推测不正确的方法为加水稀释后溶液不变红,故答案为:加水稀释后溶液不变红;
(3)强氧化性氧化漂白了红色物质,为永久性漂白,改变温度、碱的浓度均不能恢复红色,即冷却后以及加水稀释后均不变红,说明丙同学的推测正确,
故答案为:冷却后以及加水稀释后均不变红;
(4)由图可知,量筒规格未知,而过氧化钠与水的反应为放热反应,若选用装置Ⅰ,气体冷却时发生倒现象,影响测定结果,为了防止气体冷却时发生倒现象,应将导管尽量插入量筒底部,减小实验误差,应该选用装置Ⅱ测量气体体积,
故答案为:Ⅱ.
(2)乙同学的推测,与碱的浓度有关,则验证乙同学的推测不正确的方法为加水稀释后溶液不变红,故答案为:加水稀释后溶液不变红;
(3)强氧化性氧化漂白了红色物质,为永久性漂白,改变温度、碱的浓度均不能恢复红色,即冷却后以及加水稀释后均不变红,说明丙同学的推测正确,
故答案为:冷却后以及加水稀释后均不变红;
(4)由图可知,量筒规格未知,而过氧化钠与水的反应为放热反应,若选用装置Ⅰ,气体冷却时发生倒现象,影响测定结果,为了防止气体冷却时发生倒现象,应将导管尽量插入量筒底部,减小实验误差,应该选用装置Ⅱ测量气体体积,
故答案为:Ⅱ.
点评:本题考查性质实验方案的设计与评价,题目难度中等,把握习题中的信息为解答关键,注意温度、浓度的变化对颜色的影响即可解答,注重知识迁移应用,试题有利于培养学生的分析、理解能力及灵活运用所学知识的能力.

练习册系列答案
相关题目
下列各组离子,能在溶液中大量共存的是( )
| A、Na+、Cu2+、Cl-、SO42- |
| B、Na+、Ca2+、CO32-、NO3- |
| C、Na+、H+、Cl-、CO32- |
| D、K+、H+、SO42-、OH- |
已知氧化还原反应:KClO3+6HCl═3Cl2↑+KCl+3H2O,下列说法正确的是( )
| A、Cl2是氧化产物,KCl是还原产物 |
| B、盐酸在该反应中只表现还原性 |
| C、每生成3 mol Cl2,有1 mol KClO3发生氧化反应 |
| D、每转移0.1 mol电子,能生成标准状况1344mLCl2 |
当光束通过下列分散系时,可观察到丁达尔效应的是( )
| A、NaCl溶液 |
| B、H2SO4溶液 |
| C、CuSO4溶液 |
| D、Fe(OH)3胶体 |
如图所示的装置或操作正确的是( )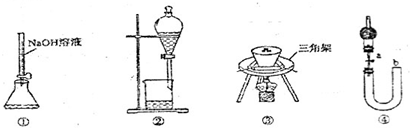

| A、用装置①量取15.00mL的NaOH溶液 |
| B、用装置②分离苯和水的混合物,苯应从下口流出 |
| C、用装置③陶瓷坩埚高温煅烧CaCO3固体 |
| D、关闭活塞a,从b处加水,以检查装置④的气密性 |
下列装置用于实验室中制取干燥氨气的实验,能达实验目的是( )

| A、用装置甲制备氨气 |
| B、用装置乙除去氨气中少量水 |
| C、用装置丙收集氨气 |
| D、用装置丁吸收多余的氨气 |
下列物质不属于合金的是( )
| A、水银 | B、青铜 | C、生铁 | D、碳素钢 |
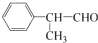 ,以苯为原料工业合成路线如下:
,以苯为原料工业合成路线如下: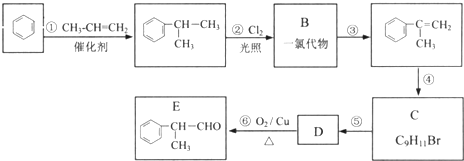
 (R-代表烃基)
(R-代表烃基)