题目内容
20.0.2mol某烃A在氧气中完全燃烧后,将产物先后通过浓硫酸和碱石灰,两者分别增重21.6g 和52.8g.试回答:(1)烃A的分子式为C6H12.
(2)若烃A能使溴水褪色,请写出比烃A少 2 个碳原子的同系物的所有同分异构体 的 结 构 简式:
 .
.
分析 n(H2O)=$\frac{21.6g}{18g/mol}$=1.2mol,n(CO2)=$\frac{52.8g}{44g/mol}$=1.2mol,由原子守恒可知,烃中C原子为$\frac{1.2mol}{0.2mol}$=6,H原子为$\frac{1.2mol×2}{0.2mpl}$=12,以此来解答.
解答 解:n(H2O)=$\frac{21.6g}{18g/mol}$=1.2mol,n(CO2)=$\frac{52.8g}{44g/mol}$=1.2mol,由原子守恒可知,烃中C原子为$\frac{1.2mol}{0.2mol}$=6,H原子为$\frac{1.2mol×2}{0.2mpl}$=12,
(1)由上述分析可知,烃A的分子式为C6H12,故答案为:C6H12;
(2)若烃A能使溴水褪色,含碳碳双键,为烯烃,比烃A少 2 个碳原子的为丁烯,其同系物的所有同分异构体的结构简式为 ,故答案为:
,故答案为: .
.
点评 本题考查有机物分子式计算的确定,为高频考点,把握有机物燃烧规律、原子守恒及同分异构体的书写为解答的关键,侧重分析与计算能力的考查,注意同系物、同分异构体的判断,题目难度不大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
8.下列说法中错误的是( )
| A. | 过滤时将液体沿着玻璃棒注入过滤器,并使液面高于滤纸边缘 | |
| B. | 蒸馏时烧瓶需要垫石棉网 | |
| C. | 当蒸发到剩余少量液体时,停止加热,利用余热将液体蒸干 | |
| D. | 冷凝管的进水方向是低进高出 |
5.某学生做如下实验:第一步,在淀粉KI溶液中滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二步,在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失.下列对实验原理的解释和所得结论错误的是( )
| A. | 蓝色逐渐消失的原因是Na2SO3溶液具有漂白性 | |
| B. | 第一步反应的离子方程式ClO-+2I-+2H+═I2+Cl-+H2O | |
| C. | 淀粉KI溶液变蓝是因为I-被氧化为I2,I2使淀粉变蓝色 | |
| D. | 微粒的氧化性由强到弱的顺序是ClO->I2>SO${\;}_{4}^{2-}$ |
12.将镁、铝各0.3mol分别放入足量的盐酸中,同温同压下产生的气体的体积比是( )
| A. | 1:1 | B. | 2:3 | C. | 3:2 | D. | 1:2 |
10.下列实验叙述中正确的是( )
| A. | 用托盘天平称量2.50 g食盐 | |
| B. | 用标准NaOH溶液滴定未知浓度盐酸,用去NaOH溶液20.50 mL | |
| C. | 用10 mL量筒量取8.25 mL盐酸 | |
| D. | 用广泛pH试纸测得某溶液pH为3.0 |
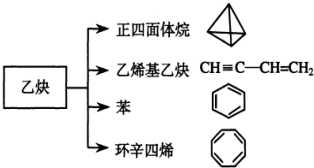

 、
、
 如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.