题目内容
5.下列各组物质中,化学键组成完全相同的是( )| A. | NaCl和NH4Cl | B. | H2CO3和K2S | C. | N2H4和C2H6 | D. | NaOH和Na2O2 |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键、非金属元素之间易形成共价键,同种非金属元素之间形成非极性共价键、不同非金属元素之间形成极性共价键,据此分析解答.
解答 解:A.NaCl中钠离子和氯离子之间只存在离子键,NH4Cl中铵根离子和氯离子之间存在离子键、N原子和H原子之间存在共价键,所以化学键类型不同,故A错误;
B.H2CO3中C原子和H原子之间、O原子和H原子之间都只存在极性键,K2S中钾离子和硫离子之间只存在离子键,所以化学键类型相同,故B错误;
C.N2H4中N原子和H原子之间存在极性键,C2H6中C原子和H原子之间存在极性键,所以化学键类型相同,故C正确;
D.NaOH中钠离子和氢氧根离子之间存在离子键、O原子和H原子之间存在极性共价键,Na2O2中钠离子和过氧根离子之间存在离子键、过氧根离子内部O原子和O原子之间存在非极性共价键,所以化学键类型不同,故D错误;
故选C.
点评 本题考查了化学键的判断,根据物质的构成微粒及微粒间的作用力来分析解答,知道离子键、共价键的区别,题目难度不大.

练习册系列答案
相关题目
16.下列容器不宜存放稀硫酸的是( )
| A. | 瓷制容器 | B. | 玻璃容器 | C. | 铁制容器 | D. | 铜制容器 |
13.下列离子方程式正确的是( )
| A. | 向CuSO4溶液中加入Na2O2:2Na2O2+Cu2++H2O═4 Na++Cu(OH)2↓+O2↑ | |
| B. | 工业上用石灰乳制备漂白粉:Ca+2OH-+Cl2=Ca2++ClO-+Cl-+H2O | |
| C. | 向Na2SiO3溶液中通入过量SO2:SiO32-+2SO2+2H2O═H2SiO3↓+2HSO3- | |
| D. | 制备Fe(OH)3胶体:Fe3++3H2O═Fe(OH)3(胶体)+3H+ |
20.下列图象分别表示有关反应的反应过程与能量变化的关系,其中判断正确的是( )
| A. | 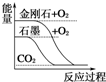 石墨转变成金刚石是吸热反应 | |
| B. | 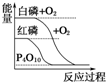 白磷比红磷稳定 | |
| C. | 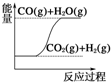 CO(g)+H2O(g)═CO2(g)+H2(g)△H>0 | |
| D. | 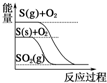 S(g)+O2(g)═SO 2(g)△H1 S(g)+O2((g)═SO2((g)△H2,则△H1>△H2 |
10.下列化学用语表示正确的是( )
| A. | NH3分子的电子式: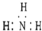 | B. | CH4分子的比例模型: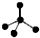 | ||
| C. | F原子的结构示意图: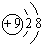 | D. | N2的结构式:N≡N |
17.下列有机反应中,不属于取代反应的是( )
| A. |  +Cl2$\stackrel{光照}{→}$ +Cl2$\stackrel{光照}{→}$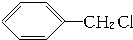 +HCl +HCl | |
| B. | CH2=CH2+Br2→CH2BrCH2Br | |
| C. | ClCH2CH═CH2+NaOH$→_{△}^{H_{2}O}$HOCH2CH═CH2+NaCl | |
| D. | 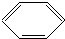 +HO-NO2$→_{△}^{浓硫酸}$ +HO-NO2$→_{△}^{浓硫酸}$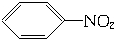 +H2O +H2O |
15.有关乙烯及其相关有机物的结构和性质,下列说法正确的是( )
| A. | 乙烯使酸性高锰酸钾褪色的原理和使溴水褪色的原理相同 | |
| B. | 乙烯不能合成高分子化合物 | |
| C. | 工业制备乙烯通常通过石油的裂解 | |
| D. | 聚乙烯能使溴水褪色 |