题目内容
(12分)某化工集团为了提高资源利用率减少环境污染,将钛厂、氯碱厂和甲醇厂组成产业链。其主要工艺如下:
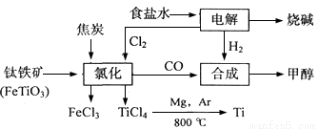
(1)写出电解食盐水反应的离子方程式 。
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式: 。
(3)已知:①Mg(s) +Cl2(g)=MgCl2(s);ΔH=-641 kJ·mol-1
②Ti(s)+2Cl2(g)=TiCl4(s);ΔH=-770 kJ·mol-1
则2Mg(s)+TiCl4(g)=2MgCl2(s)+Ti(s);ΔH
反应2Mg+TiCl4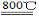 2MgCl4+Ti在Ar气氛中进行的理由是 。
2MgCl4+Ti在Ar气氛中进行的理由是 。
(4)在上述产业链中,合成192 t甲醇理论上需额外补充H2 t(不考虑生产过程中物质的任何损失)。
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是 。
(1)2Cl-+2H2O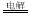 2OH-+H2↑+Cl2↑;(2分)
2OH-+H2↑+Cl2↑;(2分)
(2)2FeTiO3+6C+7Cl2 2TiCl4+2FeCl3+6CO;(2分)
2TiCl4+2FeCl3+6CO;(2分)
(3)-512 kJ?mol-1 (2分,没单位给1分)防止高温下Mg(Ti)与空气中的O2(或CO2、N2)反应;(2分)(4)10;(2分)(5)CH3OH+8OH--6e—=CO32-+6H2O(2分)
【解析】
试题分析:(1)电解食盐水生成氢氧化钠、氢气和氯气,反应的离子方程式为2Cl-+2H2O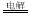 2OH-+H2↑+Cl2↑;(2)根据题给流程知,钛铁矿与焦炭、氯气反应生成氯化铁、四氯化钛和一氧化碳,化学方程式为:2FeTiO3+6C+7Cl2
2OH-+H2↑+Cl2↑;(2)根据题给流程知,钛铁矿与焦炭、氯气反应生成氯化铁、四氯化钛和一氧化碳,化学方程式为:2FeTiO3+6C+7Cl2 2TiCl4+2FeCl3+6CO;(3)已知:①Mg(s) +Cl2(g)=MgCl2(s);ΔH=-641 kJ·mol-1②Ti(s)+2Cl2(g)=TiCl4(s);ΔH=-770 kJ·mol-1,根据盖斯定律:①×2—②得2Mg(s)+TiCl4(g)=2MgCl2(s)+Ti(s);ΔH=-512 kJ?mol-1 ;反应2Mg+TiCl4
2TiCl4+2FeCl3+6CO;(3)已知:①Mg(s) +Cl2(g)=MgCl2(s);ΔH=-641 kJ·mol-1②Ti(s)+2Cl2(g)=TiCl4(s);ΔH=-770 kJ·mol-1,根据盖斯定律:①×2—②得2Mg(s)+TiCl4(g)=2MgCl2(s)+Ti(s);ΔH=-512 kJ?mol-1 ;反应2Mg+TiCl4 2MgCl4+Ti在Ar气氛中进行的理由是防止高温下Mg(Ti)与空气中的O2(或CO2、N2)反应;(4)在上述产业链中,合成甲醇的反应为:CO+2H2
2MgCl4+Ti在Ar气氛中进行的理由是防止高温下Mg(Ti)与空气中的O2(或CO2、N2)反应;(4)在上述产业链中,合成甲醇的反应为:CO+2H2 CH3OH,根据化学方程式2Cl-+2H2O
CH3OH,根据化学方程式2Cl-+2H2O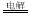 2OH-+H2↑+Cl2↑、2FeTiO3+6C+7Cl2
2OH-+H2↑+Cl2↑、2FeTiO3+6C+7Cl2 2TiCl4+2FeCl3+6CO计算合成192 t甲醇理论上需额外补充H210t;(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是CH3OH+8OH--6e—=CO32-+6H2O。
2TiCl4+2FeCl3+6CO计算合成192 t甲醇理论上需额外补充H210t;(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是CH3OH+8OH--6e—=CO32-+6H2O。
考点:以化学工艺流程为载体考查离子方程式、化学方程式及电极反应式的书写,反应热的计算,化学计算。

物质制备过程中离不开物质的提纯。以下除杂方法不正确的是
选项 | 目的 | 实验方法 |
A | 除去Na2CO3固体中的NaHCO3 | 置于坩埚中加热至恒重 |
B | 除去NaCl中少量KNO3 | 将混合物制成热饱和溶液,冷却结晶,过滤 |
C | 除去CO2中的HCl气体 | 通过NaHCO3(aq,饱和),然后干燥 |
D | 除去C2H5Br中的Br2 | 加入足量Na2SO3(aq),充分振荡,分液 |
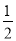 O2(g)
O2(g) SO3(g)的平衡常数K1=50,在同一温度下,反应2SO3(g)
SO3(g)的平衡常数K1=50,在同一温度下,反应2SO3(g) 2CO(正反应吸热)反应速率为v1,N2+3H2
2CO(正反应吸热)反应速率为v1,N2+3H2 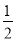 O2(g)
O2(g)  SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为  ,
, ,
,
 石墨)=
石墨)=
 石墨的总键能比1mol金刚石的总键能小1.9kJ
石墨的总键能比1mol金刚石的总键能小1.9kJ