题目内容
 X、Y、Z、Q、W为按原子序数由小到大排列的五种短周期元素,已知:
X、Y、Z、Q、W为按原子序数由小到大排列的五种短周期元素,已知:①X元素与Q处于同一主族,其原子价电子排布式都为ns2np2,且X原子半径小于Q的.
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
③Z元素的电离能数据见下表(kJ?mol-1):
请回答:
(1)XY2分子空间构型为
(2)晶体ZW的熔点比晶体XW4明显高的原因是
(3)氧化物MO的电子总数与QX的相等,则M为
(4)ZW晶体的结构示意图如图.已知:ρ(ZW)=2.2g?cm-3,NA=6.02×1023mol-1,则ZW晶体中两个最近的Z离子中心间的距离为
考点:元素电离能、电负性的含义及应用,判断简单分子或离子的构型,晶体的类型与物质熔点、硬度、导电性等的关系,晶胞的计算
专题:化学键与晶体结构
分析:X、Y、Z、Q、W为按原子序数由小到大排列的五种短周期元素,x元素与Q处于同一主族,其原子价电子排布式都为ns2np2,则x和Q属于第IVA族元素,所以X是C元素,Q是Si元素,Y元素是地壳中含量最多的元素,所以Y是O元素,w元素的电负性略小于Y元素,在W原子的电子排布中,P轨道上只有1个未成对电子,所以W是Cl元素,根据Z的电离能知,Z是第IA族元素,且Z的原子序数大于Y,所以Z是Na元素.
(1)根据价层电子对互斥理论来分析判断;
(2)根据晶体类型判断熔点的高低;
(3)离子晶体的熔点由晶格能大小决定;
(4)ZW为NaCl,根据NaCl的摩尔质量为58.5 g?mol-1及密度为2.2g?cm-3,求得晶胞的体积,进而求得棱边长,而两个距离最近的钠离子中心间的距离等于晶胞面对角线的一半,据此答题.
(1)根据价层电子对互斥理论来分析判断;
(2)根据晶体类型判断熔点的高低;
(3)离子晶体的熔点由晶格能大小决定;
(4)ZW为NaCl,根据NaCl的摩尔质量为58.5 g?mol-1及密度为2.2g?cm-3,求得晶胞的体积,进而求得棱边长,而两个距离最近的钠离子中心间的距离等于晶胞面对角线的一半,据此答题.
解答:
解:X、Y、Z、Q、W为按原子序数由小到大排列的五种短周期元素,x元素与Q处于同一主族,其原子价电子排布式都为ns2np2,则x和Q属于第IVA族元素,所以X是C元素,Q是Si元素,Y元素是地壳中含量最多的元素,所以Y是O元素,w元素的电负性略小于Y元素,在w原子的电子排布中,P轨道上只有1个未成对电子,所以W是Cl元素,根据Z的电离能知,Z是第IA族元素,且Z的原子序数大于Y,所以Z是Na元素,
(1)CO2分子中碳原子价层电子数=2+
(4-2×2)=2,且没有孤电子对,所以二氧化碳的分子空间构型为直线型,C原子的杂化方式为sp,SiC的晶体结构与金刚石的相似,每个碳原子含有4个C-Si键,所以C原子的杂化方式为sp3,碳原子和硅原子之间以共价键相结合,
故答案为:直线型;sp;sp3;共价键;
(2)一般来说,离子晶体熔点高于分子晶体,氯化钠是离子晶体,四氯化碳是分子晶体,所以晶体NaCl的熔点比晶体CCl4明显高,
故答案为:NaCl为离子晶体而CCl4为分子晶体;
(3)氧化物MO的电子总数与SiC的相等为20,则M是Mg元素,MgO是优良的耐高温材料,其晶体结构与NaCl晶体相似,相同类型的离子晶体中,晶格能与离子半径成反比,晶格能越大其熔点越高,镁离子半径小于钙离子半径,所以氧化镁的晶格能大,则MgO的熔点比CaO的高,
故答案为:Mg;Mg2+半径比Ca2+小,MgO晶格能大;
(4)ZW为NaCl,设晶胞边长为a,在NaCl晶胞中,含Cl-4个;含Na4个,根据密度公式:ρ=
,可得a=
,所以晶胞面对角线长为
?
,而两个距离最近的钠离子中心间的距离等于晶胞面对角线的一半,所以两个距离最近的钠离子中心间的距离为
?
=
×
=4.0×10-8cm;
故答案为:4.0×10-8cm.
(1)CO2分子中碳原子价层电子数=2+
| 1 |
| 2 |
故答案为:直线型;sp;sp3;共价键;
(2)一般来说,离子晶体熔点高于分子晶体,氯化钠是离子晶体,四氯化碳是分子晶体,所以晶体NaCl的熔点比晶体CCl4明显高,
故答案为:NaCl为离子晶体而CCl4为分子晶体;
(3)氧化物MO的电子总数与SiC的相等为20,则M是Mg元素,MgO是优良的耐高温材料,其晶体结构与NaCl晶体相似,相同类型的离子晶体中,晶格能与离子半径成反比,晶格能越大其熔点越高,镁离子半径小于钙离子半径,所以氧化镁的晶格能大,则MgO的熔点比CaO的高,
故答案为:Mg;Mg2+半径比Ca2+小,MgO晶格能大;
(4)ZW为NaCl,设晶胞边长为a,在NaCl晶胞中,含Cl-4个;含Na4个,根据密度公式:ρ=
| ||
| a3 |
| 3 |
| ||
| 2 |
| 3 |
| ||
| ||
| 2 |
| 3 |
| ||
| ||
| 2 |
| 3 |
| ||
故答案为:4.0×10-8cm.
点评:本题考查物质结构及其性质,正确推断元素是解本题关键,利用价层电子对互斥理论分析分子空间构型及杂化方式,为考试热点,晶胞的有关计算为本题的难点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述正确的是( )
| A、12g石墨烯(单层石墨)中含有六元环的个数为0.5NA |
| B、25℃时pH=13的NaOH溶液中含有OH一的数目为0.1 NA |
| C、1mol的羟基与1 mol的氢氧根离子所含电子数均为9 NA |
| D、1.0L 1.5mo1?L-1的NaAlO2水溶液中含有的氧原子数为3NA |
下列叙述中,错误的是( )
| A、微粒半径由大到小顺序是:F->Na+>H+ |
| B、在NaCl晶体中每个Na+(或Cl-)周围都紧邻6个Cl-(或Na+) |
| C、白磷晶体中,分子之间通过共价键结合,键角为60° |
| D、离子晶体在熔化时,离于键被破坏,而分子晶体熔化时,化学键不被破坏 |
下列实验装置能够达到目的是( )
A、 检验溴乙烷在NaOH乙醇溶液加热的产物 |
B、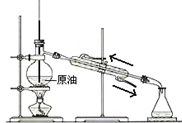 石油的分馏 |
C、 分离乙醇和乙酸的混合物 |
D、 实验室制取乙酸乙酯 |
 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.