题目内容
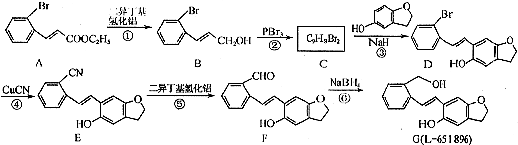
11.化合物G是一种抗精神病药物,可以通过下列方法合成: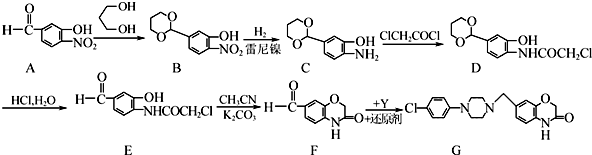
(1)
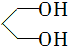 的名称为1,3丙二醇;设计步骤A→B的目的是保护醛基,防止被还原.
的名称为1,3丙二醇;设计步骤A→B的目的是保护醛基,防止被还原.(2)E→F的反应类型是取代反应.
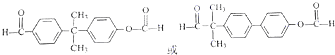
(3)Y的分子式为C10H13N2Cl,则Y的结构简式为
 .
.(4)写出同时满足下列条件的C的一种同分异构体的结构简式:
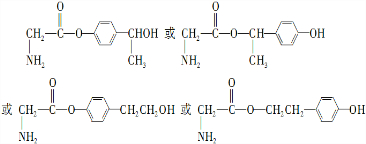 .
.①苯环上有两个取代基;
②核磁共振氢谱图中有7个峰;
③能发生水解反应,产物之一是氨基乙酸,另一种产物能与FeCl3溶液发生显色反应.
(5)已知:①
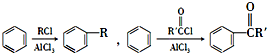
②
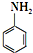 易氧化,酰胺基(
易氧化,酰胺基(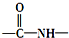 )难以被H2还原.
)难以被H2还原.化合物Z(
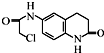 )是合成一种新型口服强心药的中间体,请写出以
)是合成一种新型口服强心药的中间体,请写出以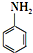 、ClCH2CH2COCl、ClCH2COCl为原料制备Z的合成路线流程图(无机试剂可任选).
、ClCH2CH2COCl、ClCH2COCl为原料制备Z的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:
CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓硫酸,△}^{CH_{3}CH_{2}CHOH}$CH3COOCH2CH3.
分析 (1)属于二元醇,指明羟基位置进行命名;B中硝基被氢气还原转化为C中氨基,A转化B的目的是保护醛基,防止被还原;
(2)对比E、F的结构可知,E脱去1分子HCl形成F,属于取代反应;
(3)对比F、G的结构,结合Y的分子式为C10H13N2Cl,可知Y的结构简式为 ;
;
(4)同时满足下列条件的C的一种同分异构体:①苯环上有两个取代基,②核磁共振氢谱图中有7个峰,③能发生水解反应,可以含有酯基,产物之一是氨基乙酸,可以含有氨基,另一种产物能与FeCl3溶液发生显色反应,可以含有酚羟基,或者羧酸与酚形成的酯基;
(5)苯胺先与ClCH2CH2COCl发生取代反应生成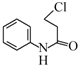 ,然后再氯化铝作用下生成
,然后再氯化铝作用下生成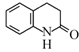 ,发生硝化反应生成
,发生硝化反应生成 ,再发生还原反应生成
,再发生还原反应生成 ,最后与ClCH2COCl发生取代反应生成
,最后与ClCH2COCl发生取代反应生成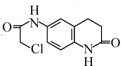 .
.
解答 解:(1)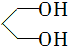 的名称为1,3丙二醇,B中硝基被氢气还原转化为C中氨基,A转化B的目的是保护醛基,防止被还原,
的名称为1,3丙二醇,B中硝基被氢气还原转化为C中氨基,A转化B的目的是保护醛基,防止被还原,
故答案为:1,3丙二醇;保护醛基,防止被还原;
(2)对比E、F的结构可知,E脱去1分子HCl形成F,属于取代反应,
故答案为:取代反应;
(3)对比F、G的结构,结合Y的分子式为C10H13N2Cl,可知Y的结构简式为 ,
,
故答案为: ;
;
(4)同时满足下列条件的C的一种同分异构体:①苯环上有两个取代基,②核磁共振氢谱图中有7个峰,③能发生水解反应,可以含有酯基,产物之一是氨基乙酸,可以含有氨基,另一种产物能与FeCl3溶液发生显色反应,可以含有酚羟基,或者羧酸与酚形成的酯基,符合条件的同分异构体为: ,
,
故答案为: ;
;
(5)苯胺先与ClCH2CH2COCl发生取代反应生成 ,然后再氯化铝作用下生成
,然后再氯化铝作用下生成 ,发生硝化反应生成
,发生硝化反应生成 ,再发生还原反应生成
,再发生还原反应生成 ,最后与ClCH2COCl发生取代反应生成
,最后与ClCH2COCl发生取代反应生成 ,合成路线流程图为:
,合成路线流程图为: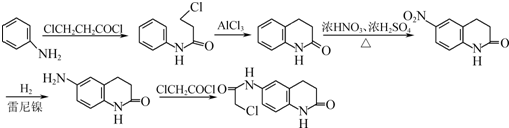 ,
,
故答案为: .
.
点评 本题考查有机物的合成,注意根据转化关系及给予的信息进行合成路线设计,侧重考查学生自学能力、信息获取与迁移运用能力,(4)中同分异构体的书写为易错点、难点,熟练掌握官能团的性质与衍变.

 初中暑期衔接系列答案
初中暑期衔接系列答案| A. | 食用蛋白质可以为人体提供氨基酸 | |
| B. | 加碘盐中的碘是I2 | |
| C. | 袋装食品里放置的小袋硅胶是抗氧化剂 | |
| D. | 发酵粉中的小苏打是Na2CO3 |
| A. | 氟离子的结构示意图: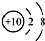 | |
| B. | 次氯酸的结构式:H-Cl-O | |
| C. | 溴化铵的电子式: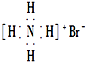 | |
| D. | 质子数为53,中子数为78的碘原子:53131 I |
| A. | 漂白粉中加入浓盐酸:ClO-+Cl-+2H+═Cl2↑+H2O | |
| B. | 氯化铁溶液洗涤银镜:Fe3++Ag═Fe2++Ag+ | |
| C. | 0.1 mol•L-1NH4HSO4溶液和0.1 mol•L-1NaOH等体积混合:NH4++H++2OH-═NH3•H2O+H2O | |
| D. | 0.1 mol•L-1的NaAlO2溶液和0.15 mol•L-1的H2SO4溶液等体积混合:AlO2-+4H+═Al3++2H2O |
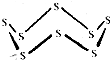 黑火药是我国古代的四大发明之一,KNO3、C及S8 (结构式如图所示)爆炸生成K2S、CO2和N2,下列说法正确的是( )
黑火药是我国古代的四大发明之一,KNO3、C及S8 (结构式如图所示)爆炸生成K2S、CO2和N2,下列说法正确的是( )| A. | 该反应属于置换反应 | |
| B. | 该反应中氧化剂只有KNO3 | |
| C. | 32g S8含有S-S的数目约为6.02×1023 | |
| D. | 1mol KNO3参与该反应,转移电子总数目约为5×6.02×1023 |
Ⅰ.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照下表所示的方案完成实验.
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL 2%H2O2溶液 | 无 |
| ② | 10mL 5%H2O2溶液 | 无 |
| ③ | 10mL 5%H2O2溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ④ | 10mL 5%H2O2溶液+少量HCl溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL 5%H2O2溶液+少量NaOH溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
同学们进行实验时没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进方法是向反应物中加入等量同种催化剂(或将盛有反应物的试管放在同一热水浴中)(填一种即可).
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图甲所示.
分析该图能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.
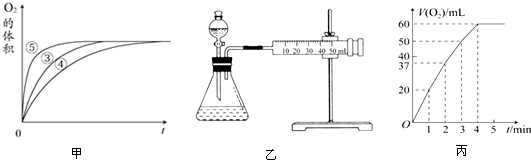
Ⅱ.资料显示,某些金属离子对H2O2的分解起催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,该实验小组的同学设计了如图乙所示的实验装置进行实验.
(1)某同学通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量单位时间生成O2的体积或生成单位体积O2所需要的时间来比较;
(2)0.1g MnO2粉末加入50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图丙所示.解释反应速率变化的原因:随着反应的进行,浓度减小,反应速率减慢,计算H2O2的初始物质的量浓度为0.11mol/L.(保留两位有效数字,在标准状况下测定)
(3)根据化学反应速率与化学平衡理论,联系化工生产实际,你认为下列说法不正确的是C(填序号).
A.化学反应速率理论可以指导怎样在一定时间内快出产品
B.勒夏特列原理可以指导怎样使有限原料多出产品
C.催化剂的使用是提高产品产率的有效办法
D.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益.
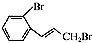 .
. (只写一种).
(只写一种).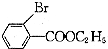 为原料制备二氢异苯并呋喃(结构简式如图
为原料制备二氢异苯并呋喃(结构简式如图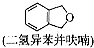 )的合成路线流程图(无机试剂可任选).
)的合成路线流程图(无机试剂可任选).