题目内容
在一个容积固定为2L的密闭容器中,发生反应:aA (g)+bB(g)?pC(g)△H=?反应情况记录如下表:
请根据表中数据仔细分析,回答下列问题:
(1)第2min到第4min内A的平均反应速率V(A)= mol?L-1?min-1
(2)由表中数据可知反应在第4min到第6min时处于平衡状态,若在第2min、第6min、第8min时分别改变了某一个反应条件,则改变的条件分别可能是:
①第2min 或 ;
②第6min ;
③第8min .
(3)若从开始到第4min建立平衡时反应放出的热量为235.92kJ则该反应的△H= .
(4)反应在第4min建立平衡,此温度下该反应的化学平衡常数K= .
| 时间/(min) | n(A)/( mol) | n(B)/( mol) | n(C)/( mol) |
| 0 | 1 | 3 | 0 |
| 第2min | 0.8 | 2.6 | 0.4 |
| 第4min | 0.4 | 1.8 | 1.2 |
| 第6min | 0.4 | 1.8 | 1.2 |
| 第8min | 0.1 | 2.0 | 1.8 |
| 第9min | 0.05 | 1.9 | 0.3 |
(1)第2min到第4min内A的平均反应速率V(A)=
(2)由表中数据可知反应在第4min到第6min时处于平衡状态,若在第2min、第6min、第8min时分别改变了某一个反应条件,则改变的条件分别可能是:
①第2min
②第6min
③第8min
(3)若从开始到第4min建立平衡时反应放出的热量为235.92kJ则该反应的△H=
(4)反应在第4min建立平衡,此温度下该反应的化学平衡常数K=
考点:化学平衡的计算,化学平衡建立的过程
专题:化学平衡专题
分析:(1)在相同时间段内,各物质的浓度的变化量之比即为方程式的系数之比;A物质的化学反应速率v(A)=
,代入数据进行计算即可;
(2)影响化学反应速率的因素有:使用催化剂、改变温度、浓度、改变物质的表面积等;
(3)在开始到第4min建立平衡时,A物质的消耗量为0.6mol/(l?min),根据化学方程式计算即可;
(4)以及平衡常数计算公式计算即可.
| △cA |
| △t |
(2)影响化学反应速率的因素有:使用催化剂、改变温度、浓度、改变物质的表面积等;
(3)在开始到第4min建立平衡时,A物质的消耗量为0.6mol/(l?min),根据化学方程式计算即可;
(4)以及平衡常数计算公式计算即可.
解答:
解:(1)在前2min内,各物质的浓度的变化量之比(1-0.8):(3-2.6):(0.4-0)=1:2:2,即,方程式的系数分别为:1、2、2;A物质的化学反应速率v(A)=
=
=0.1mol/(l?min),故答案为:0.1;
(2)①在第0~2min内,A的浓度减小了0.2mol/l,在2~4min内A的浓度在原基础上减小了0.4mol/l,化学反应速率加快了,可以是使用催化剂或升高温度,故答案为:使用催化剂或升高温度;
②第6min 到第8min,作为反应物,浓度应该是减小的趋势,但是B的浓度从1.8mol/l增加到了2.0mol/l,所以可知一定是加入了B物质,故答案为:增加B的浓度;
③第8min到第9min时间段内,C作为生成物,它的浓度应是增大的趋势,但是数据表明,其浓度减小了,一定是减少了C的浓度,故答案为:减小C的浓度.
(3)根据热化学方程式,设:反应的焓变值为X
A(g)+2B(g)?2C(g)△H=-XkJ/mol
1mol XkJ
(
mol/L-0.2mol/l)×2L 235.92kJ
则有:
=
,解得:X=-393.2 kJ?mol-1
故答案为:-393.2kJ?mol-1;
(4)依据方程式:K=
=
=2.22,故答案为:2.22.
| △cA |
| △t |
| ||
| 2min |
(2)①在第0~2min内,A的浓度减小了0.2mol/l,在2~4min内A的浓度在原基础上减小了0.4mol/l,化学反应速率加快了,可以是使用催化剂或升高温度,故答案为:使用催化剂或升高温度;
②第6min 到第8min,作为反应物,浓度应该是减小的趋势,但是B的浓度从1.8mol/l增加到了2.0mol/l,所以可知一定是加入了B物质,故答案为:增加B的浓度;
③第8min到第9min时间段内,C作为生成物,它的浓度应是增大的趋势,但是数据表明,其浓度减小了,一定是减少了C的浓度,故答案为:减小C的浓度.
(3)根据热化学方程式,设:反应的焓变值为X
A(g)+2B(g)?2C(g)△H=-XkJ/mol
1mol XkJ
(
| 1 |
| 2 |
则有:
| 1mol |
| 0.6mol |
| XkJ |
| 235.92kJ |
故答案为:-393.2kJ?mol-1;
(4)依据方程式:K=
| c2(C) |
| c(A)?c2(B) |
| 0.62 |
| 0.2×0.92 |
点评:本题主要考查了影响化学反应速率的因素和有关反应速率的计算、化学平衡常数的定义以及计算等,难度较大,有一定的综合性,熟练掌握三段法是解决此类题是关键.

练习册系列答案
相关题目
下列关于有机物的叙述中,正确的是( )
| A、天然植物油常温下一般呈液态,难溶于水,有固定的熔沸点 |
| B、煤油可由石油分馏获得,常用作燃料和保存少量金属钠 |
| C、乙酸、乙醇分子中都含有羟基,均能被氧化为乙醛 |
| D、苯和HNO3的反应与乙烯和Br2的反应属于同一类型的反应 |
氯化银在水中存在沉淀溶解平衡,25℃时,氯化银的Ksp=1.8×10-10.现将足量氯化银分别放入:①100mL蒸馏水中;②100mL 0.1mol?L-1盐酸中;③100mL 0.1mol?L-1氯化铝溶液中,充分搅拌后,在相同温度下,c(Ag+)由大到小的顺序是( )
| A、①②③ | B、③②① |
| C、②①③ | D、②③① |
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 淀粉(氯化钠) | 蒸馏水 | 渗析 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| D | 乙烷(乙烯) | 氢气 | 加热 |
| A、A | B、B | C、C | D、D |
对于某合成材料(如塑料制品)废弃物的处理方法中正确的是( )
| A、将废弃物混在垃圾中填埋在土壤中 |
| B、将废弃物焚烧 |
| C、将废弃物用化学方法加工成涂料或汽油 |
| D、将废弃物倾倒在海洋中 |
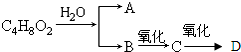

 的所有原子
的所有原子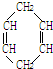 可简写为
可简写为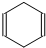 .现有某化合物W的分子结构可表示为
.现有某化合物W的分子结构可表示为 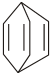 .
.