题目内容
8.下列有关仪器的使用正确的是( )| A. | 手持试管给试管内的物质加热 | |
| B. | 稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 | |
| C. | 用天平称量药品时用手直接拿砝码 | |
| D. | 用滴管滴加液体时滴管应垂直悬垂在容器上方且不能触及容器内壁 |
分析 A.手持试管给试管内的物质加热会将手烫伤;
B.稀释浓硫酸时,应将浓硫酸沿烧杯壁缓慢注入水中,并用玻璃棒不断搅拌;
C.使用托盘天平时,不能用手拿砝码,应该用镊子;
D.应将胶头滴管垂悬在试管上方.
解答 解:A.用试管夹从试管底由下往上夹住距试管口约$\frac{1}{3}$处,手持试管夹长柄末端,进行加热,故A错误;
B.稀释浓硫酸时,应将浓硫酸沿烧杯壁缓慢注入水中,并用玻璃棒不断搅拌,防止液体溅出伤人,故B错误;
C.使用托盘天平时,用手拿砝码,应该用镊子,否则容易使砝码锈蚀,故C错误;
D.向试管中滴加溶液时应将胶头滴管垂悬在试管上方,不能伸入试管内,故D正确.
故选D.
点评 本题考查化学实验的基本操作,题目难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
16.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1:1 | |
| B. | 常温下,0.1 mol•L-1 NH4NO3溶液中含有的氮原子数是0.2NA | |
| C. | 常温常压下,3.2 g O2和3.2 g O3所含氧原子数都是0.2NA | |
| D. | 1mol 甲基所含电子数约为10NA |
3.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,22.4 L氯水含有NA个Cl2分子 | |
| B. | 在1 L 0.1 mol•L-1碳酸钠溶液中阴离子总数大于0.1NA | |
| C. | 50 mL18.4 mol•L-1浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA | |
| D. | 标准状况下,由H2O2制得4.48 LO2转移的电子数目为0.8NA |
13.设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 3.4gNH3中含N-H键数目为0.2NA | |
| B. | 标准状况下,体积相同的两种气体的分子数一定相同 | |
| C. | 标准状况下,22.4L甲醇中含有的氧原子数目为1.0NA | |
| D. | 1L0.1mol•L-1的Fe2(SO4)3溶液中,Fe3+的数目为0.2NA |
20.如图装置中(烧杯中均盛有海水),铁不易被腐蚀的是( )
| A. |  | B. | 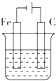 | C. |  | D. |  |
18.下列说法正确的是( )
| A. | 物质的量是七个基本物理量之一,符号为mol | |
| B. | 摩尔质量在数值上等于该物质的相对分子质量或相对相对原子质量 | |
| C. | 标准状况下,气体的摩尔体积为22.4L | |
| D. | 11.7克氯化钠溶于1000毫升水中,所得溶质的物质的量浓度为0.2mol•L-1 |
 A、B、C、D、E、F、G为前四周期元素.A、B最外层电子排布可表示为asa、bsbbpb(a≠b);C元素对应单质是空气中含量最多的物质;D的最外层电子数是内层电子数的3倍;E与D同主族,且位于D的下一周期;F与E同周期,且是本周期中电负性最大的元素:基态G原子核外电子填充在7个能级中,且价层电子均为单电子.
A、B、C、D、E、F、G为前四周期元素.A、B最外层电子排布可表示为asa、bsbbpb(a≠b);C元素对应单质是空气中含量最多的物质;D的最外层电子数是内层电子数的3倍;E与D同主族,且位于D的下一周期;F与E同周期,且是本周期中电负性最大的元素:基态G原子核外电子填充在7个能级中,且价层电子均为单电子. .
.

 ,.
,. ,
, ,
, ,
, .
.

 .
. 、
、 .
.