题目内容
7.苯环结构中不存在C-C单键与C=C双键的交替结构,可以作为证据的是( )①苯能使溴水萃取分层
②苯不能使酸性高锰酸钾溶液褪色
③苯在一定条件下既能发生取代反应,又能发生加成反应
④经测定,邻二甲苯只有一种结构
⑤经测定,苯环上碳碳键的键长相等.
| A. | ④⑤ | B. | ①②③⑤ | C. | ①②③ | D. | ②④⑤ |
分析 ①②③根据碳碳双键的性质判断;
④根据同分异构体数目解答;
⑤单、双键不同,键长不相等,据此分析.
解答 解:①苯能使溴水萃取分层,体现了有机溶剂的物理性质,故①错误;
②苯不能使酸性高锰酸钾溶液褪色,说明苯分子中不含碳碳双键,可以证明苯环结构中不存在C-C单键与C=C双键的交替结构,故②正确;
③苯能在一定条件下跟H2加成生成环己烷,发生加成反应是双键具有的性质,不能证明苯环结构中不存在C-C单键与C=C双键的交替结构,故③错误;
④如果是单双键交替结构,邻二甲苯的结构有两种,一种是两个甲基夹C-C,另一种是两个甲基夹C=C.邻二甲苯只有一种结构,说明苯环结构中的化学键只有一种,不存在C-C单键与C=C双键的交替结构,故④正确;
故选D.
点评 本题考查苯的结构与性质,难度不大,综合性较大,要求学生知识掌握全面,能运用知识分析和解决问题,重在能力的考查.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
17.下列关于烃性质的说法中正确的是( )
| A. | 乙烯可以与酸性高锰酸钾溶液反应,因此可以用酸性高锰酸钾溶液除去乙烷中混有的乙烯 | |
| B. | 溴乙烷可以通过乙烯与溴化氢加成得到,也可以通过乙烷与溴发生取代反应制备 | |
| C. | 区分甲苯和苯可以使用酸性高锰酸钾溶液,也可以用溴水 | |
| D. | 鉴别己烯中是否混有少量甲苯,正确的实验方法是可以加足量溴水,然后再加入酸性高锰酸钾溶液 |
2.由C5H10、C3H6O2和C6H12O6组成的混合物,经测定含氧元素的质量分数为x,则此混合物中含碳元素的质量分数为( )
| A. | $\frac{6(1-x)}{7}$ | B. | $\frac{1-x}{7}$ | C. | $\frac{3x}{4}$ | D. | 无法计算 |
12.下列混合溶液中,各离子浓度的大小顺序正确的是( )
| A. | 10 mL 0.1 mol•L-1氨水与10 mL 0.1 mol•L-1盐酸混合,c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | 10 mL 0.1 mol•L-1NH4Cl溶液与5 mL 0.2 mol•L-1NaOH溶液混合,c(Na+)=c(Cl-)>c(OH-)>c(H+) | |
| C. | 10 mL 0.1 mol•L-1CH3COOH溶液与5 mL 0.2 mol•L-1NaOH溶液混合,c(Na+)=c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 10 mL 0.5 mol•L-1CH3COONa溶液与6 mL 1 mol•L-1盐酸混合,c(Cl-)>c(Na+)>c(OH-)>c(H+) |
16.对SO2与SO3说法正确的是( )
| A. | 都是直线形结构 | |
| B. | 中心原子都采取sp3杂化轨道 | |
| C. | SO2中S原子和SO3中S原子上都没有孤对电子 | |
| D. | SO2为V形结构,SO3为平面三角形结构 |
17.下表是元素周期表的一部分.
根据A一K元素在周期表中的位置用具体的化学式回答.
(1)原子半径最小的是H,能形成化合物种类最多的是C.
(2)最高价氧化物对应水化物中,酸性最强的是HClO4,表现两性的是Al(OH)3.以上两种化合物相互反应的离子方程为3H++Al(OH)3=Al3++3H2O.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | E | F | H | I | K | |||
| 3 | B | C | D | G | J |
(1)原子半径最小的是H,能形成化合物种类最多的是C.
(2)最高价氧化物对应水化物中,酸性最强的是HClO4,表现两性的是Al(OH)3.以上两种化合物相互反应的离子方程为3H++Al(OH)3=Al3++3H2O.
 在1.5L的密闭容器中通入2molX2和3molY2的混合气体,在一定条件下发生反应:X2(g)+3Y2(g)?2Z(g)+4W(?)△H<0达到平衡时,容器内压强为反应开始时的0.8(相同温度下测量).
在1.5L的密闭容器中通入2molX2和3molY2的混合气体,在一定条件下发生反应:X2(g)+3Y2(g)?2Z(g)+4W(?)△H<0达到平衡时,容器内压强为反应开始时的0.8(相同温度下测量).
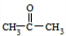 +2H2O;
+2H2O;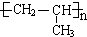 .
.