题目内容
16.写出下列物质发生水解反应的离子方程式(1)Na2CO3溶液中滴加酚酞呈红色,原因是CO32-+H2O?HCO3-+OH-(用离子方程式表示),加热后颜色变深
(2)CH3COONa溶液PH>7(填“>”“<”或“=”),原因是CH3COO-+H2O?CH3COOH+OH-(用离子方程式表示)
(3)普通泡沫灭火器内的玻璃筒里-盛硫酸铝溶液,铁筒里-盛碳酸氢钠溶液,其化学反应的原理是Al3++3HCO3-═Al(OH)3↓+3CO2↑
(用离子方程式表示),不能把硫酸铝溶液盛在铁筒里的原因是(用离子方程式表示)Al3++3H2O?Al(OH)3+3H+.
分析 (1)Na2CO3为强碱弱酸盐,在溶液中存在水解平衡CO32-+H2O?HCO3-+OH-,盐类水解吸热;
(2)CH3COONa属于强碱弱酸盐,醋酸根水解,破坏水的电离平衡,溶液呈碱性;
(3)Al3+与3HCO3-发生互促水解反应,生成氢氧化铝沉淀和二氧化碳气体,据此写出离子方程式;硫酸铝水解显酸性.
解答 解:(1)Na2CO3为强碱弱酸盐,水解呈碱性,在溶液中存在CO32-+H2O?HCO3-+OH-,水解过程为吸热过程,加热温度升高,使CO32-水解平衡右移,c(OH-)增大,溶液碱性增强,所以红色加深,
故答案为:CO32-+H2O?HCO3-+OH-;深;
(2)CH3COONa属于强碱弱酸盐,醋酸根水解CH3COO-+H2O?CH3COOH+OH-,破坏水的电离平衡,溶液呈碱性,溶液的pH>7,
故答案为:>;CH3COO-+H2O?CH3COOH+OH-;
(3)Al3+与3HCO3-发生互促水解反应,反应为Al3++3HCO3-═Al(OH)3↓+3CO2↑,产生大量二氧化碳气体,可用于灭火;硫酸铝水解显酸性Al3++3H2O?Al(OH)3+3H+,故不能用铁桶盛放.
故答案为:Al3++3HCO3-═Al(OH)3↓+3CO2↑;Al3++3H2O?Al(OH)3+3H+.
点评 本题考查盐类水解的应用,题目涉及盐类的互促水解,侧重于考查学生综合运用化学知识的能力,题目难度中等.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
6.部分弱酸的电离平衡常数如表:下列选项错误的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 (25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A. | 2HCOOH+CO32-═2HCOO-+H2O+CO2↑ | |
| B. | 2CN-+H2O+CO2═2HCN+CO32- | |
| C. | 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者 | |
| D. | HCOO-和CN-结合H+能力前者小于后者 |
5.某同学设计如图1所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:
(1)实验过程中,使用分液漏斗滴加液体的操作是打开分液漏斗上口的活塞(或将活塞上的凹槽与瓶口上的小孔对齐),旋开分液漏斗的旋塞,缓慢滴加.
(2)该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?不可行(填“可行”或“不可行”).原因为NO会与装置中空气反应,生成NO2溶于水,使测得的NO气体体积不准
(3)实验Ⅲ烧瓶中产生的SO2气体通入溴水溶液中发生反应的离子方程式是SO2+Br2+2H2O=4H++2Br-+SO42-.
(4)实验Ⅱ中量气管中的液体最好是c(填字母编号,下同).
a.浓NaOH溶液 b.氨水 c.煤油 d.氯化铵溶液
该实验剩余的NH3需吸收处理.如图2,以下各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有ACDF.
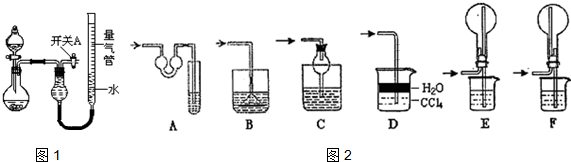
(5)本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,②使量气管两端液面相平,③视线与凹液面最低处相平.
(6)实验Ⅳ获得以下数据(所有气体体积已换算成标准状况,忽略滴入液体体积对气体体积的影响)
根据上述数据,可计算出镁铝合金中铝的质量分数为27.0%.(H:1 Mg:24 Al:27)
| 实验 | 药品 | 制取气体 | 量气管中的液体 |
| Ⅰ | Cu、稀HNO3 | H2O | |
| Ⅱ | NaOH固体、浓氨水 | NH3 | |
| Ⅲ | Na2SO3固体、浓H2SO4 | SO2 | |
| Ⅳ | 镁铝合金、NaOH溶液(足量) | H2 | H2O |
(2)该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?不可行(填“可行”或“不可行”).原因为NO会与装置中空气反应,生成NO2溶于水,使测得的NO气体体积不准
(3)实验Ⅲ烧瓶中产生的SO2气体通入溴水溶液中发生反应的离子方程式是SO2+Br2+2H2O=4H++2Br-+SO42-.
(4)实验Ⅱ中量气管中的液体最好是c(填字母编号,下同).
a.浓NaOH溶液 b.氨水 c.煤油 d.氯化铵溶液
该实验剩余的NH3需吸收处理.如图2,以下各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有ACDF.

(5)本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,②使量气管两端液面相平,③视线与凹液面最低处相平.
(6)实验Ⅳ获得以下数据(所有气体体积已换算成标准状况,忽略滴入液体体积对气体体积的影响)
| 编号 | 镁铝合金度量 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 1.0g | 10.0mL | 346.3mL |
| ② | 1.0g | 10.0mL | 335.0mL |
| ③ | 1.0g | 10.0mL | 345.7mL |
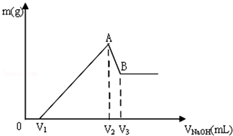 将Mg、Al组成的混合物共0.1mol溶于100mL 3mol/LHCl溶液中,再滴加1mol/LNaOH 溶液,在滴加NaOH溶液的过程中,沉淀的质量m随NaOH溶液体积V的变化如图所示:
将Mg、Al组成的混合物共0.1mol溶于100mL 3mol/LHCl溶液中,再滴加1mol/LNaOH 溶液,在滴加NaOH溶液的过程中,沉淀的质量m随NaOH溶液体积V的变化如图所示: