题目内容
9.有甲、乙两醋酸稀溶液,测得甲的PH=2,乙的PH=3,下列推断中正确的是( )| A. | 物质的量浓度C(甲)=C(乙) | |
| B. | 甲中由水电离产生的H+的物质的量浓度是乙的0.1倍 | |
| C. | 中和等物质的量浓度等体积的NaOH溶液需甲、乙两酸的体积V(乙)=10V(甲) | |
| D. | 甲中的C(OH-)为乙中C(OH-)的10倍 |
分析 醋酸为弱电解质,在醋酸溶液中存在电离平衡,且醋酸溶液越稀,其电离程度越大,酸电离的氢离子浓度越大,水电离程度越小,据此分析.
解答 解:A.如果醋酸的电离程度相等,则物质的量浓度c(甲)=10c(乙),实际上乙的电离程度大于甲,所以c(甲)>10c(乙),故A错误;
B.甲中水电离出的氢离子=$\frac{{K}_{w}}{0.01}$,乙中水电离出的氢离子浓度=$\frac{{K}_{w}}{0.001}$,所以甲中由水电离产生的H+的物质的量浓度是乙的0.1倍,故B正确;
C.因为c(甲)>10c(乙),所以中和等物质的量浓度等体积的NaOH溶液需甲、乙两酸的体积V(乙)>10V(甲),故C错误;
D.甲中氢氧根离子浓度=$\frac{{K}_{w}}{0.01}$,乙中氢氧根离子浓度=$\frac{{K}_{w}}{0.001}$,所以甲氢氧根离子浓度是乙的0.1倍,故D错误;
故选B.
点评 本题考查弱电解质电离,明确弱电解质溶液的浓稀与其电离程度之间的关系是解本题关键,难度不大.

练习册系列答案
相关题目
19.下列实验操作或装置正确的是( )
| A. | 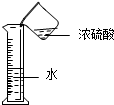 稀释浓硫酸 | B. |  排水集气法收集NO | ||
| C. |  分离水与 酒精 | D. | 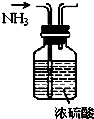 干燥氨气 |
17.下列除去杂质的方法不 正确的是( )
| A. | 用过量烧碱溶液除去镁粉中混有少量铝粉 | |
| B. | 用过量氨水除去Fe3+溶液中的少量Al3+ | |
| C. | 用加热方法除去Na2CO3中混有少量NaHCO3 | |
| D. | 用过量氢氧化钠溶液除去MgO中的少量Al2O3 |
1.化学与生活密切相关.下列生活中常见物质的俗名与化学式相对应的是( )
| A. | 纯碱-NaHCO3 | B. | 胆矾-CuSO4 | C. | 醋酸-CH3COOH | D. | 生石灰-CaCO3 |
18.“保护环境”是我国的基本国策.下列做法不应该提倡的是( )
| A. | 对生活废弃物进行分类处置 | B. | 过度开发资源促进经济发展 | ||
| C. | 煤炭燃烧时安装“固硫”装置 | D. | 宣传“低碳”出行 |
19.2015年8月12日天津港瑞海公司危险化学品仓库发生特大火灾爆炸事故,事故警示我们,化学药品的安全存放是非常重要的.下列有关化学药品的存放说法不正确的是( )
| A. | 液溴易挥发,应用少量的水液封并放在冷暗处保存 | |
| B. | 碳酸钠虽然属于盐,但是其水溶液呈碱性,应用带橡胶塞的试剂瓶保存 | |
| C. | 金属钠遇到氧气和水均立即反应,应保存在煤油里 | |
| D. | 硝酸见光易分解、易挥发,应用棕色广口试剂瓶密封保存 |
 已知X、Y和Z三种元素的原子序数之和等于42.X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子.X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子.请回答下列问题:
已知X、Y和Z三种元素的原子序数之和等于42.X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子.X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子.请回答下列问题: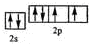 ;
;