题目内容
11.下列化学用语表述正确的是( )| A. | 质子数为53、中子数为78的碘原子:131 53I | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | 一个D2O分子所含的中子数为8 | |
| D. | N2的电子式:N:::N: |
分析 A.质量数=质子数+中子数,元素符号的最简式为质量数、左下角为质子数;
B.乙烯的结构简式中漏掉了碳碳双键;
C.D2O分子中含有中子数为:1×2+8=10;
D.氮气分子中的3对共用电子对的表示方法错误.
解答 解:A.质子数为53、中子数为78的碘原子的质量数为131,该原子可以表示为:13153I,故A正确;
B.乙烯分子中存在碳碳双键,乙烯正确的结构简式为:CH2=CH2,故B错误;
C.D原子中含有1个中子,则一个D2O分子所含的中子数为:1×2+8=10,故C错误;
D.氮原子为成键的孤对电子对未画出,氮气分子电子式为 ,故D错误;
,故D错误;
故选A.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、元素符号、结构简式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
1.2005年 10月12日,我国成功发射了神州六号载人飞船,下列可用在飞船生活舱中给宇航员提供氧气的物质是( )
| A. | KMnO4 | B. | KClO3 | C. | Na2O2 | D. | MnO2 |
2.下列物质中,属于电解质的是( )
| A. | 铜片 | B. | 硫酸溶液 | C. | 氯化钠 | D. | 酒精 |
19.少量铁粉与100ml0.01mol•L-1的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法的( )
①加H2O
②滴入几滴浓HNO3
③滴入几滴浓盐酸
④加CH3COONa固体
⑤加NaCl溶液
⑥升高温度(不考虑盐酸挥发)
⑦改用10mL 0.1mol•L-1的盐酸
⑧用铁片代替铁粉
⑨滴加少量CuSO4溶液.
①加H2O
②滴入几滴浓HNO3
③滴入几滴浓盐酸
④加CH3COONa固体
⑤加NaCl溶液
⑥升高温度(不考虑盐酸挥发)
⑦改用10mL 0.1mol•L-1的盐酸
⑧用铁片代替铁粉
⑨滴加少量CuSO4溶液.
| A. | ①⑥⑦ | B. | ③⑥⑦ | C. | ③⑤⑦ | D. | ⑤⑥⑦ |
6.X,Y,Z,M,W为原子序数依次增大的5种短周期元素.X的质子总数与电子层数相同,Y,Z,M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍.Z与其同主族的短周期元素可形成常见的大气污染气体甲.X,Y,Z三种元素形成化合物乙.下列说法错误的是( )
| A. | 气体甲可与Z的某种氢化物反应生成强酸 | |
| B. | W元素的晶体单质是一种良好的半导体材料 | |
| C. | X分别与Y,Z,M,W形成的常见化合物中,稳定性最好的是XM | |
| D. | 化合物乙中一定只有共价键 |
3.为确定下列置于空气中的物质是否变质,所选检验试剂(括号内物质)不能达到目的是( )
| A. | Na2SO3溶液(BaCl2) | B. | FeCl2溶液(KSCN) | ||
| C. | 海带灰过滤所得的溶液(淀粉溶液) | D. | NaOH溶液(CaCl2) |
20.下列反应的离子方程式书写正确的是( )
| A. | NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+OH-+Ba2+═H2O+BaCO3↓ | |
| B. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -═2 Al(OH)3↓+3BaSO4↓ | |
| C. | 向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| D. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ |
13.下列各表述与示意图一致的是( )
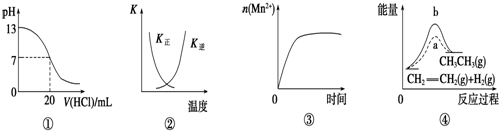

| A. | 图①表示25℃时,用0.1 mol/L盐酸滴定20 mL 0.1 mol/L NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. | 图②中曲线表示反应2SO2(g)+O2(g)?2SO3(g)△H<0正、逆反应的平衡常数K随温度的变化 | |
| C. | 图③表示10 mL 0.01 mol/L KMnO4酸性溶液与过量的0.1 mol/L H2C2O4溶液混合时,n(Mn2+)随时间的变化 | |
| D. | 图④中a、b曲线分别表示反应:CH2═CH2(g)+H2(g)→CH3CH3(g)△H<0使用和未使用催化剂时,反应过程中的总能量变化 |
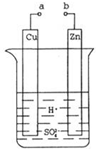 原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.
原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.