题目内容
12.下列电离方程式错误的是( )①NaHCO3═Na++H++CO32-
②NaHSO4═Na++H++SO42-
③H2SO4═2H++SO42-
④KClO3═K++Cl-+3O2-.
| A. | ①② | B. | ① | C. | ①④ | D. | ③④ |
分析 ①HCO3-是H2CO3的酸式盐的酸根部分,部分电离;
②NaHSO4是强酸强碱酸式盐,完全电离出Na+、H+、SO42-离子;
③H2SO4是强电解质,完全一步电离生成硫酸根离子、氢离子;
④氯酸钾是强电解质,是由钾离子和氯酸根离子构成,氯酸根离子不能拆写.
解答 解:①NaHCO3是H2CO3的酸式盐,HCO3-不能拆,电离方程式为:NaHCO3═Na++HCO3-,故①错误;
②NaHSO4是强酸强碱酸式盐,属强电解质,完全电离用“═”,电离出Na+、H+、SO42-离子,其电离方程式为:NaHSO4=Na++H++SO42-,故②正确;
③硫酸为二元强酸,一步完全电离,电离方程式为:H2SO4═2H++SO42-,故③正确;
④氯酸钾是强电解质,是由钾离子和氯酸根离子构成,能完全电离,电离方程式为:KClO3=K++ClO3-,故④错误;
故选C.
点评 本题考查了电离方程式的书写判断,掌握正确书写电离方程式的方法,并会正确判断电离方程式的正误是解题的关键,题目难度不大.

练习册系列答案
相关题目
2.下表为几种短周期元素的性质:( )
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-1nm) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低化合价 | -2 | -3 | -1 | -3 |
| A. | 元素⑤的氢化物沸点高于元素①的氢化物 | |
| B. | ③④处于同一周期 | |
| C. | 上述八种元素中,最高价氧化物对应水化物的酸性最强的是元素⑤ | |
| D. | ⑧号元素位于周期表中第三周期第ⅢA族 |
20.下列半径比较正确的是( )
| A. | Na、Mg、Ca原子半径从大到小 | B. | O2-、Na+、K+半径从小到大 | ||
| C. | Cl、Cl- 半径前者大 | D. | H、N、Al 半径从小到大 |
7.能证明乙醇分子中含有一个羟基的事实是( )
| A. | 1mol乙醇完全燃烧生成3mol水 | |
| B. | 乙醇能与水以任意比例互溶 | |
| C. | 乙醇沸点较高 | |
| D. | 0.1mol乙醇与足量金属钠反应生成0.05molH2 |
2.下列化学用语中,正确的是( )
| A. | 乙烯的结构简式CH2CH2 | B. | NaCl的电子式  | ||
| C. | CO2分子的结构式O-C-O | D. | Mg原子结构示意图 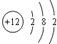 |
 .
. .
. .
.