题目内容
某无色溶液中,若加入NaClO溶液或适量稀盐酸,均能产生淡黄色沉淀,则该溶液中可能大量存在的离子是
- A.Na+、K+、S2-、Cl-
- B.H+、Na+、S2-、NO
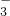
- C.K+、Ca2+、S2-、SO
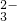
- D.Na+、S2-、SO
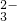 、SO
、SO
D
分析:根据离子之间不能结合生成水、沉淀、气体,则离子不能共存,结合加入NaClO溶液或适量稀盐酸,均能产生淡黄色沉淀,以此来解答.
解答:A.该组离子之间不反应,能共存,但加盐酸不生成沉淀,故A不选;
B.因H+、S2-、NO3-发生氧化还原反应,则不能共存,故B不选;
C.因Ca2+、SO32-结合生成沉淀,则不能共存,故C不选;
D.该组离子之间不反应,能共存,且加入NaClO溶液与S2-发生氧化还原反应生成S,加适量稀盐酸H+、S2-、SO32-发生氧化还原反应生成S,均能产生淡黄色沉淀,故D选;
故选D.
点评:本题考查离子的共存,熟悉习题中的氧化还原反应为解答本题的关键,注意离子的性质即可解答,题目难度不大.
分析:根据离子之间不能结合生成水、沉淀、气体,则离子不能共存,结合加入NaClO溶液或适量稀盐酸,均能产生淡黄色沉淀,以此来解答.
解答:A.该组离子之间不反应,能共存,但加盐酸不生成沉淀,故A不选;
B.因H+、S2-、NO3-发生氧化还原反应,则不能共存,故B不选;
C.因Ca2+、SO32-结合生成沉淀,则不能共存,故C不选;
D.该组离子之间不反应,能共存,且加入NaClO溶液与S2-发生氧化还原反应生成S,加适量稀盐酸H+、S2-、SO32-发生氧化还原反应生成S,均能产生淡黄色沉淀,故D选;
故选D.
点评:本题考查离子的共存,熟悉习题中的氧化还原反应为解答本题的关键,注意离子的性质即可解答,题目难度不大.

练习册系列答案
相关题目