题目内容
3.在固定容积的密闭容器中进行如下反应:2A(g)+B(g)?2C(g),已知反应过程某一时刻A,B,C浓度分别为0.2mol•L-1,0.1mol•L-1,0.2mol•L-1,达到平衡时浓度可能正确的是( )| A. | A,B分别为0.4mol•L-1,0.2mol•L-1 | B. | A为0.25mol•L-1 | ||
| C. | A,C均为0.15mol•L-1 | D. | A为0.24mol•L-1,C为0.14mol•L-1 |
分析 化学平衡的建立,既可以从正反应开始,也可以从逆反应开始,或者从正逆反应开始,不论从哪个方向开始,物质都不能完全反应,利用极限法假设完全反应,计算出相应物质的浓度变化量,实际变化量小于极限值,据此判断分析.
解答 解:A、A和B的浓度增大,说明反应向逆反应方向进行建立平衡,若C完全反应,则SO2和O2的浓度浓度变化分别为0.2mol/L、0.1mol/L,而实际变化等于该值,故A错误;
B、A浓度增大,说明反应向逆反应方向进行建立平衡,若C完全反应,则A的浓度浓度变化为0.2mol/L,而实际变化小于该值,故B正确;
C、反应物、生产物的浓度不可能同时增大,应一个减小,另一个一定增大,故C错误;
D、C的浓度减少,说明该反应向逆反应方向进行建立平衡,C浓度变为0.14mol•L-1,则参与反应的C浓度变为0.06mol•L-1,则A的浓度的浓度变化为0.06mol/L,浓度变为0.26mol•L-1,故D错误.
故选B.
点评 本题考查了化学平衡的建立,难度不大,关键是利用可逆反应的不完全性,运用极限假设法解答,假设法是解化学习题的常用方法.

练习册系列答案
相关题目
13.需加入适当的氧化剂才能实现的反应是( )
| A. | Fe2O3→Fe3O4 | B. | Na2S4→Na2S2 | C. | S2O32-→S4O62- | D. | Cl3-→Cl- |
15.环己双妥明是一种新型的纤维酸类降脂新药,可由有机物X通过一步反应而制得:
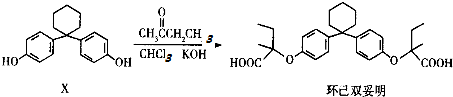
下列有关叙述正确的是( )

下列有关叙述正确的是( )
| A. | 有机物X的分子式为C18H22O2 | |
| B. | 有机物X与环己双妥明互为同系物 | |
| C. | 环己双妥明苯环上的一氯代物有4种 | |
| D. | 环己双妥明能与碳酸氢钠溶液发生反应 |