题目内容
下列各项中“操作或现象”能达到预期“实验目的”的是( )
| 选项 | 操作或现象 | 实验目的 |
| A | 向AlCl3溶液中加入过量的NaOH溶液,过滤,洗涤,干燥,加热灼烧 | 制取Al2O3 |
| B | 用饱和的Na2CO3溶液可以将BaSO4转化为BaCO3 | 证明Ksp(BaSO4)>Ksp(BaCO3) |
| C | 在氯化氢气氛中加热蒸发MgCl2溶液 | 制取无水MgCl2 |
| D | 将SO2通入品红溶液中,品红溶液褪色,加热褪色后的品红溶液,溶液恢复红色 | 验证H2SO3的不稳定性 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.Al(OH)3不溶于弱碱,但能溶于强碱;
B.当Qc>Ksp时,生成沉淀;
C.氯化镁易水解生成氢氧化镁和HCl,为防止氯化镁水解应该将氯化镁溶液在HCl气氛中加热蒸发;
D.二氧化硫具有漂白性,但其漂白性不稳定.
B.当Qc>Ksp时,生成沉淀;
C.氯化镁易水解生成氢氧化镁和HCl,为防止氯化镁水解应该将氯化镁溶液在HCl气氛中加热蒸发;
D.二氧化硫具有漂白性,但其漂白性不稳定.
解答:
解:A.Al(OH)3不溶于弱碱,但能溶于强碱NaOH,应该用氯化铝和氨水制取Al(OH)3,然后灼烧Al(OH)3制取Al2O3,故A错误;
B.用饱和的Na2CO3溶液可以将BaSO4转化为BaCO3,是因为Qc>Ksp时,生成沉淀,与沉淀转化无关,Ksp(BaSO4)<Ksp(BaCO3),故B错误;
C.氯化镁易水解生成氢氧化镁和HCl,升高温度促进水解,为防止氯化镁水解应该将氯化镁溶液在HCl气氛中加热蒸发,故C正确;
D.二氧化硫具有漂白性,但其漂白性不稳定,加热后易恢复原来颜色,与亚硫酸稳定性大小无关,故D错误;
故选C.
B.用饱和的Na2CO3溶液可以将BaSO4转化为BaCO3,是因为Qc>Ksp时,生成沉淀,与沉淀转化无关,Ksp(BaSO4)<Ksp(BaCO3),故B错误;
C.氯化镁易水解生成氢氧化镁和HCl,升高温度促进水解,为防止氯化镁水解应该将氯化镁溶液在HCl气氛中加热蒸发,故C正确;
D.二氧化硫具有漂白性,但其漂白性不稳定,加热后易恢复原来颜色,与亚硫酸稳定性大小无关,故D错误;
故选C.
点评:本题考查化学实验方案评价,侧重考查反应原理,明确物质性质是解本题关键,知道二氧化硫和次氯酸漂白原理区别,易错选项是B,
常见实验评价试题类型有:
a.评价实验原理
b.评价实验方法
c.评价药品、仪器
d.评价实验现象和结论.
常见实验评价试题类型有:
a.评价实验原理
b.评价实验方法
c.评价药品、仪器
d.评价实验现象和结论.

练习册系列答案
相关题目
下列实验装置图所示的实验操作,能达到相应的实验目的是( )
A、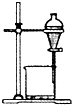 分离酒精和水 |
B、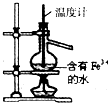 获得少量蒸馏水 |
C、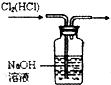 除去Cl2中的HCl |
D、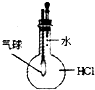 证明HCl易溶于水 |
用NA表示阿伏加德常数,下列叙述中正确的是( )
A、在标准状况下,1L庚烷完全燃烧后,所生成的气态产物的分子数为
| ||
| B、1mol碳正离子CH5+所含的电子数为10NA | ||
| C、标准状况下,16g甲烷完全燃烧所消耗的氧气的分子数的3NA | ||
| D、0.5molC3H8分子中含C-H共价键2NA |
I2(g)+H2(g)?2HI(g)△H<0,在其他条件不变的情况下正确说法是( )
| A、加入催化剂,改变了反应的途径,反应的△H也随之改变 |
| B、改变压强,平衡不发生移动,反应放出的热量不变 |
| C、升高温度,反应速率加快,反应放出的热量变多 |
| D、若在原电池中进行,反应放出的热量不变 |
如图是某硫酸试剂瓶标签上的部分内容,据此判断下列说法不正确的是( )


| A、该硫酸的物质的量浓度为l8.4mol/L |
| B、该硫酸与等体积的水混合所得溶液的质量分数大于49% |
| C、配制200.0mL4.6mol/L的稀硫酸需取该硫酸50.0mL |
| D、6.4gCu与足量的该硫酸充分反应产生的气体一定为2.24L |
下列叙述中正确的是( )
| A、某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+ |
| B、液溴易挥发,在存放液溴的试剂瓶中应加水封 |
| C、某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- |
| D、能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 |
最高正化合价是它的负化合价的3倍的那一族元素是( )
| A、第ⅦA族 | B、第ⅥA族 |
| C、第ⅤA族 | D、第ⅢA族 |
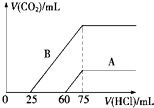 取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题: