题目内容
13.(1)系统命名法命名下列物质①
 乙苯
乙苯②
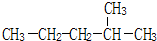 2-甲基戊烷
2-甲基戊烷③
 2,3-二甲基戊烷
2,3-二甲基戊烷④
 4-甲基-2-戊烯
4-甲基-2-戊烯⑤
 3,3-二甲基-1-丁炔.
3,3-二甲基-1-丁炔.
分析 判断有机物的命名是否正确或对有机物进行命名,其核心是准确理解命名规范:
1)命名要符合“一长、一近、一多、一小”,也就是主链最长,编号起点离支链最近,支链数目要多,支链位置号码之和最小;
2)有机物的名称书写要规范;
3)对于结构中含有苯环的,命名时可以依次编号命名,也可以根据其相对位置,用“邻”、“间”、“对”进行命名.
4)含有官能团的有机物命名时,要选含官能团的最长碳链作为主链,官能团的位次最小.
解答 解:①苯环连接乙基,是苯的同系物,名称为:乙苯,
故答案为:乙苯;
②是烷烃主链有5个碳原子,从离甲基近的一端编号,名称为:2-甲基戊烷,
故答案为:2-甲基戊烷;
③是烷烃主链有5个碳原子,从离甲基近的一端编号,名称为:2,3-二甲基戊烷,
故答案为:2,3-二甲基戊烷;
④为烯烃,选取含双键在内的最长碳链为主链,含4个碳原子,从离双键近的一端开始编号,写出名称为:4-甲基-2-戊烯,
故答案为:4-甲基-2-戊烯;
⑤为炔烃,选取含三键在内的最长碳链为主链,含4个碳原子,从离三键近的一段开始编号,写出名称为:3,3-二甲基-1-丁炔,
故答案为:3,3-二甲基-1-丁炔.
点评 本题考查了有机物的命名知识.一般要求了解烷烃的命名、苯的同系物的命名及简单的烃的衍生物的命名.命名时要遵循命名原则,书写要规范,题目难度不大.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
17.能够快速、微量、精确的测定有机物相对分子质量的物理方法是( )
| A. | 核磁共振谱 | B. | 红外光谱 | C. | 质谱 | D. | 紫外光谱 |
18.甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整.向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
回答下列问题:
(1)反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H=-41.2kJ/mol.
(2)在初始阶段,甲烷蒸汽重整的反应速率小于甲烷氧化的反应速率(填大于、小于或等于).
(3)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应CH4(g)+H2O(g)?CO(g)+3H2(g)KP的表达式为$\frac{{p}^{3}({H}_{2})p(CO)}{p(C{H}_{4})p({H}_{2}O)}$;随着温度的升高,该平衡常数增大(填“增大”、“减小”或“不变”).
(4)从能量角度分析,甲烷自热重整方法的先进之处在于系统内强放热的甲烷氧化反应为强吸热的蒸汽重整反应提供了所需的能量.
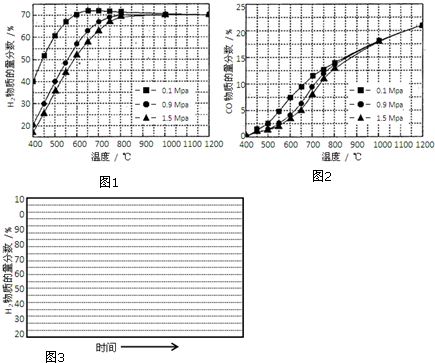
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如图1、2:
①若要达到H2物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是B.
A.600℃,0.9Mpa B.700℃,0.9MPa C.800℃,1.5MpaD.1000℃,1.5MPa
②画出600℃,0.1Mpa条件下,系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图3:
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是甲烷氧化程度过高,导致生成的氢气和氧气反应.
| 反应 过程 | 化学方程式 | 焓变△H (kJ/mol) | 正反应活化能Ea (kJ/mol) |
| 甲烷 氧化 | CH4(g)+2O2(g)=CO2(g)+2H2O(g) | -802.6 | 125.6 |
| CH4(g)+O2(g)=CO2(g)+2H2(g) | -322.0 | 172.5 | |
| 蒸汽 重整 | CH4(g)+H2O(g)=CO(g)+3H2(g) | 206.2 | 240.1 |
| CH4(g)+2H2O(g)=CO2(g)+4H2(g) | 165.0 | 243.9 |
(1)反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H=-41.2kJ/mol.
(2)在初始阶段,甲烷蒸汽重整的反应速率小于甲烷氧化的反应速率(填大于、小于或等于).
(3)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应CH4(g)+H2O(g)?CO(g)+3H2(g)KP的表达式为$\frac{{p}^{3}({H}_{2})p(CO)}{p(C{H}_{4})p({H}_{2}O)}$;随着温度的升高,该平衡常数增大(填“增大”、“减小”或“不变”).
(4)从能量角度分析,甲烷自热重整方法的先进之处在于系统内强放热的甲烷氧化反应为强吸热的蒸汽重整反应提供了所需的能量.
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如图1、2:
①若要达到H2物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是B.
A.600℃,0.9Mpa B.700℃,0.9MPa C.800℃,1.5MpaD.1000℃,1.5MPa
②画出600℃,0.1Mpa条件下,系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图3:
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是甲烷氧化程度过高,导致生成的氢气和氧气反应.

1.下列事实能说明乙酸(CH3COOH) 属于弱酸的是( )
①1mol/L CH3COOH的 pH=2
②乙酸能与水以任意比互溶
③20mL 1mol/L CH3COOH 与20mL 1mol/LNaOH恰好中和
④CH3COONa溶液的pH>7.
①1mol/L CH3COOH的 pH=2
②乙酸能与水以任意比互溶
③20mL 1mol/L CH3COOH 与20mL 1mol/LNaOH恰好中和
④CH3COONa溶液的pH>7.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
8.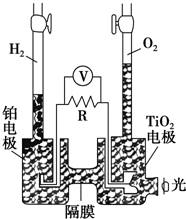 TiO2在光照射下可使水分解:2H2O $\frac{\underline{\;TiO_{2}\;}}{\;}$2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( )
TiO2在光照射下可使水分解:2H2O $\frac{\underline{\;TiO_{2}\;}}{\;}$2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( )
 TiO2在光照射下可使水分解:2H2O $\frac{\underline{\;TiO_{2}\;}}{\;}$2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( )
TiO2在光照射下可使水分解:2H2O $\frac{\underline{\;TiO_{2}\;}}{\;}$2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( )| A. | 该装置可以将光能转化为电能,同时也能将其转化为化学能 | |
| B. | TiO2电极上发生的反应为:2H++2e-═H2↑ | |
| C. | 该装置工作时,电流由TiO2电极经R流向铂电极 | |
| D. | 该装置工作时,TiO2电极附近溶液的pH变大 |
18.分子式为C9H10O2的芳香族化合物并且能与饱和NaHCO3溶液反应放出气体的有机物有(不含立体异构)( )
| A. | 6种 | B. | 8种 | C. | 12种 | D. | 14种 |
5.下列判断正确的是( )
| A. | 酸酐一定是氧化物 | |
| B. | 酸性氧化物一定是非金属氧化物 | |
| C. | 碱性氧化物一定是金属氧化物 | |
| D. | 正四面体分子中键角一定是109°28′ |
2.某气态烃0.5mol恰好与1molHCl加成,1mol生成物又可与6mol Cl2发生取代反应.则此烃可能是( )
| A. | C2H2 | B. | CH2=CHCH=CH2 | C. | CH≡C-CH3 | D. | CH≡C-CH2-CH3 |
3.下列有关碱金属元素的说法正确的是( )
| A. | 锂与过量氧气反应,生成过氧化锂 | B. | 从锂到铯,密度由小到大 | ||
| C. | 从锂到铯,熔沸点依次升高 | D. | 钠与水反应不如钾与水反应剧烈 |