题目内容
Li-CuO电池是一种新型绿色电池.它的比能量高、电压高、工作温度宽,使用寿命比其他类型电池长,特别适合于大电流、重负载放电应用.该电池的总反应为:2Li+CuO=Li2O+Cu,电解质溶液为高氯酸锂有机溶液.下列说法正确的是( )(Li的相对原子质量:7)
| A、电池的正极反应式为:CuO+2e-+2Li+=Li2O+Cu |
| B、常温时,在正负极间接上电流表,指针不偏转 |
| C、放电过程中,Li+向负极移动 |
| D、每转移0.1mol电子,理论上消耗1.4gLi |
考点:原电池和电解池的工作原理
专题:
分析:A、根据电池的总反应为:2Li+CuO=Li2O+Cu,正极发生的是CuO的得电子的反应过程;
B、根据电池反应能产生电流,则在正负极间接上电流表,指针偏转;
C、放电过程中,Li+向正极移动;
D、根据电池反应和电子转移情况来计算.
B、根据电池反应能产生电流,则在正负极间接上电流表,指针偏转;
C、放电过程中,Li+向正极移动;
D、根据电池反应和电子转移情况来计算.
解答:
解:A、电池的总反应为:2Li+CuO=Li2O+Cu,正极发生的是CuO的得电子的反应过程,电极反应为:CuO+2e-+2Li+=Li2O+Cu,故A正确;
B、由电池的总反应为:2Li+CuO=Li2O+Cu能产生电流,则在正负极间接上电流表,指针偏转,故B错误;
C、放电过程中,Li+向正极移动,故C错误;
D、根据电池反应:2Li+CuO=Li2O+Cu,当电池转移0.1mol电子,理论上消耗0.7gLi,故D错误;
故选A.
B、由电池的总反应为:2Li+CuO=Li2O+Cu能产生电流,则在正负极间接上电流表,指针偏转,故B错误;
C、放电过程中,Li+向正极移动,故C错误;
D、根据电池反应:2Li+CuO=Li2O+Cu,当电池转移0.1mol电子,理论上消耗0.7gLi,故D错误;
故选A.
点评:本题是一道有关新型绿色电池的工作原理的综合题目,要求学生熟悉教材基本知识,具备分析和解决问题的能力.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
用光洁的铂丝蘸取某无色溶液,在无色火焰上灼烧时,观察到黄色火焰,则无色溶液中一定含有( )
| A、Cu2+ |
| B、K+ |
| C、Na+ |
| D、Ba2+ |
某一反应物在一定条件下的平衡转化率为25.3%,当使用了催化剂时,其转化率为( )
| A、大于25.3% |
| B、小于25.3% |
| C、等于25.3% |
| D、不能确定 |
下列说法正确的是( )
| A、RO3-与R-可发生反应:RO3-+5R-+6H+══3R2+3H2O,元素R位于周期表中第ⅤⅡA族 |
| B、短周期主族元素的最高价等于最外层电子数 |
| C、原子序数越大原子半径越大,离子半径越小 |
| D、第三周期元素随原子序数增大,含氧酸的酸性增强 |
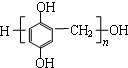 单体是
单体是 单体是
单体是 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题: