题目内容
4.下列有关说法正确的是( )| A. | CaCO3(s)═CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 | |
| B. | 镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | |
| C. | N2(g)+3H2(g)═2NH3(g)△H<0,其他条件不变时升高温度,反应速率v(H2)和H2的平衡转化率均增大 | |
| D. | 水的离子积常数Kw 随着温度的升高而增大,说明水的电离是吸热反应 |
分析 A.△H-T△S>0,室温下不能自发进行,该反应的△S>0;
B.镀铜铁制品镀层受损后,构成原电池时Fe为负极;
C.△H<0,其他条件不变时升高温度,平衡逆向移动;
D.Kw与温度有关.
解答 解:A.△H-T△S>0,室温下不能自发进行,该反应的△S>0,则△H>T△S>0,故A错误;
B.镀铜铁制品镀层受损后,构成原电池时Fe为负极,电化学腐蚀大于化学腐蚀的速率,则铁制品比受损前更容易生锈,故B正确;
C.△H<0,其他条件不变时升高温度,平衡逆向移动,则H2的平衡转化率减小,但反应速率加快,故C错误;
D.Kw与温度有关,则Kw 随着温度的升高而增大,说明水的电离是吸热反应,故D正确;
故选BD.
点评 本题考查较综合,涉及反应热与焓变、电化学腐蚀、平衡移动等,为高频考点,把握反应中能量变化、原电池原理、平衡移动影响因素为解答的关键,侧重分析与应用能力的考查,注意化学反应原理的应用,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.下列说法中错误的是( )
| A. | 乙烷和乙烯的熔点都比CH4的高 | B. | 乙烷和乙烯都可发生加成反应 | ||
| C. | 乙烷能发生氧化反应 | D. | 苯和乙烯都是常见化工原料 |
12.元素性质呈周期性变化的决定因素是( )
| A. | 元素原子半径大小呈周期性变化 | |
| B. | 元素原子量依次递增 | |
| C. | 元素原子核外电子排布呈周期性变化 | |
| D. | 元素的最高正化合价呈周期性变化 |
19.有六种微粒分别是1940X、2040Y、1840Z、1940Q+、2040K2+、2040M,它们所属元素的种类为( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
9.常温下,醋酸和氨水的电离平衡常数均为1.8×10-5.向10mL浓度为0.1mol•L-1的NH3•H2O溶液中滴加相同浓度的CH3COOH(温度变化忽略不计),在滴加过程中( )
| A. | c(NH4+)与c(NH3•H2O)之和始终保持不变 | |
| B. | 水的电离程度始终增大 | |
| C. | $\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$始终减小 | |
| D. | 当加入CH3COOH的体积为10mL时,溶液pH>7 |
16.下列化学用语正确的是( )
| A. | 核内有8个中子的碳原子:$\stackrel{8}{6}$ C | B. | 氯离子的结构示意图: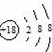 | ||
| C. | HCl的电子式: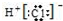 | D. | 甲烷分子的比例模型: |
13.以下转化能通过一步反应实现的是( )
| A. | Al2O3→Al(OH)3 | B. | Al→Na[Al (OH)4] | C. | Fe→Fe(OH)2 | D. | SiO2→H2SiO3 |
14.2008年,我国的航天事业取得了巨大的成就,航天员翟志刚顺利实现了太空行走.下列说法不正确的是( )
| A. | 在生活舱中,可用过氧化钠制备氧气 | |
| B. | 金属镁可用作制造飞机、火箭的重要材料 | |
| C. | 在航天试验用的仪器仪表中大量使用了硅等非金属材料 | |
| D. | 返回舱外层的隔热瓦使用的是金属材料 |
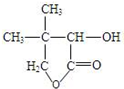 G的合成线路如图:
G的合成线路如图: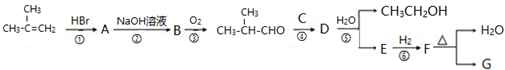
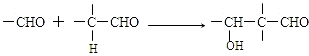
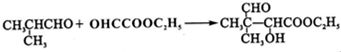 .
.