题目内容
12.下列物质的用途不正确的是( )| A | B | C | D | |
| 物质 | 硅  | 生石灰  | 液氨 | 亚硝酸钠 |
| 用途 | 半导体材料 | 抗氧化剂 | 制冷剂 | 食品防腐剂 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.硅导电性介于导体与半导体之间;
B.生石灰具有吸水性;
C.液氨汽化吸收大量的热;
D.亚硝酸盐具有还原性.
解答 解:A.硅导电性介于导体与半导体之间,是良好的半导体材料,故A正确;
B.生石灰具有吸水性,生石灰用作食品干燥剂,不具有还原性,不能做抗氧剂,故B错误;
C.液氨汽化吸收大量的热,具有制冷作用,可做制冷剂,故C正确;
D.亚硝酸盐具有还原性,可做防腐剂,故D正确;
故选:B.
点评 本题考查了物质的用途,性质决定用途,明确相关物质的性质是解题关键,题目难度不大.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
3.下列有关实验的说法不正确的是( )
| A. | 容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶都无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| B. | 在4mL0.1mol•L-1的K2Cr2O7溶液中滴加数滴1mol•L-1的NaOH溶液,溶液颜色从橙色变成黄色 | |
| C. | 在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用,迅速混合后测出初始温度,用环形玻璃搅拌棒进行搅拌使酸和碱充分反应、准确读取实验时温度计最高温度、并且取2-3 次的实验平均值等措施,以达到良好的实验效果 | |
| D. | 将含有少量氯化钾的硝酸钾放入烧杯中,加水溶解并加热、搅拌,当溶液表面出现一层晶膜时停止加热,冷却结晶,过滤即可得到大量硝酸钾晶体 |
7.电解质量分数为5.2%的NaOH溶液1L(密度为1.06g/cm3),用铂作电极电解,当溶液中NaOH的质量分数改变了1.0% 时停止电解,此时溶液中符合下表关系的是( )
| NaOH的质量分数 | 阳极析出物质的质量/g | 阴极析出物质的质量/g | |
| A | 6.2% | 19 | 152 |
| B | 6.2% | 152 | 19 |
| C | 4.2% | 1.2 | 9.4 |
| D | 4.2% | 9.4 | 1.2 |
| A. | A | B. | B | C. | C | D. | D |
4.常温常压下,断裂1mol(理想)气体分子化学键所吸收的能量或形成1mol(理想)气体分子化学键所放出的能量称为键能(单位为KJ.mol-1)下表是一些键能数据(KJ•mol-1)
回答下列问题:
(1)由表中数据规律预测C-Br键的键能范围:218 kJ•mol-1<C-Br键能<330 kJ•mol-1.
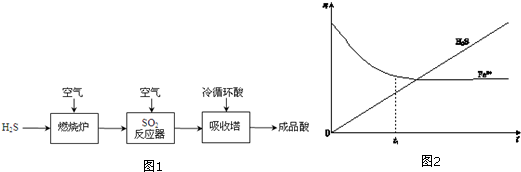
(2)写出H2(g)与S2(g)反应生成H2S(g)的热化学方程式2H2(g)+S2(g)═2H2S(g)△H=-229kJ•mol-1.
| 化学键 | 键能 | 化学键 | 键能 | 化学键 | 键能 |
| C-F | 427 | C-Cl | 330 | C-I | 218 |
| H-H | 436 | S=S | 255 | H-S | 339 |
(1)由表中数据规律预测C-Br键的键能范围:218 kJ•mol-1<C-Br键能<330 kJ•mol-1.
(2)写出H2(g)与S2(g)反应生成H2S(g)的热化学方程式2H2(g)+S2(g)═2H2S(g)△H=-229kJ•mol-1.
1.分子式为C7H6O2的芳香族化合物的数目有( )
| A. | 2种 | B. | 3种 | C. | 4 | D. | 5种 |
2.下列说法正确的是( )
| A. | 蔗糖在人体内水解的最终产物是葡萄糖 | |
| B. | 蔬菜水果属于碱性食物,对人体健康有益 | |
| C. | 为了防止蛋白质发生盐析,疫苗等生物制剂要冷藏 | |
| D. | 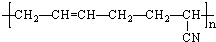 由CH2=CH2与CH2=CH-CN加聚而成 由CH2=CH2与CH2=CH-CN加聚而成 |
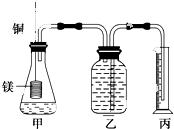 某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的二元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图.该实验的主要操作步骤如下:
某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的二元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图.该实验的主要操作步骤如下: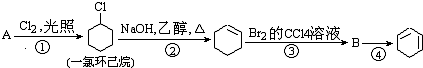
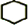 ,名称是环己烷.
,名称是环己烷. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$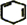 +2NaBr+2H2O.
+2NaBr+2H2O.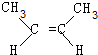 、
、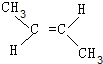 .
.