题目内容
 实验室需要配制0.50mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.
实验室需要配制0.50mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.(1)选择仪器.完成本实验所必需的仪器有:托盘天平(精确到0.1g)、药匙、烧杯、玻璃棒、
(2)计算.配制该溶液需取NaCl晶体
(3)称量.①称量过程中NaCl晶体应放于天平的
②称量完毕,将药品倒入烧杯中.
(4)溶解、冷却.
(5)转移、洗涤.在转移时应使用
(6)定容,摇匀.
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配制的时间、溶液名称及浓度.
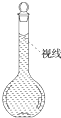
(8)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会
考点:配制一定物质的量浓度的溶液
专题:物质的量浓度和溶解度专题
分析:(1)根据配制步骤是计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(2)根据n=cV和m=nM来计算;
(3)用托盘天平称量药品时,要注意左物右码;
(5)为了防止溶液溅出,要用玻璃棒引流;洗涤烧杯并将洗涤液注入容量瓶的目的是将溶质都转移至容量瓶;
(8)根据c=
并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析.
(2)根据n=cV和m=nM来计算;
(3)用托盘天平称量药品时,要注意左物右码;
(5)为了防止溶液溅出,要用玻璃棒引流;洗涤烧杯并将洗涤液注入容量瓶的目的是将溶质都转移至容量瓶;
(8)根据c=
| n |
| V |
解答:
解:(1)操作步骤有计算、称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.由于无480ml的容量瓶,故选用500ml容量瓶,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管.
根据提供的仪器可知,还需仪器有500ml容量瓶、胶头滴管,
故答案为:500mL容量瓶、胶头滴管;
(2)由于无480ml的容量瓶,故选用500ml容量瓶,故配制出的溶液的体积为500ml.根据n=cV可知需要的NaCl的物质的量n=0.50mol/L×0.5L=0.25mol,质量m=nM=0.25mol×58.5g/mol=14.6g,故答案为:14.6;
(3)用托盘天平称量药品时,应左物右码,故答案为:左盘;
(5)为了防止溶液溅出,要用玻璃棒引流;洗涤烧杯并将洗涤液注入容量瓶的目的是将溶质都转移至容量瓶,故答案为:玻璃棒;将溶质全部转移至容量瓶;
(8)仰视刻度线,会导致溶液体积偏大,则浓度偏低,故答案为:偏低.
根据提供的仪器可知,还需仪器有500ml容量瓶、胶头滴管,
故答案为:500mL容量瓶、胶头滴管;
(2)由于无480ml的容量瓶,故选用500ml容量瓶,故配制出的溶液的体积为500ml.根据n=cV可知需要的NaCl的物质的量n=0.50mol/L×0.5L=0.25mol,质量m=nM=0.25mol×58.5g/mol=14.6g,故答案为:14.6;
(3)用托盘天平称量药品时,应左物右码,故答案为:左盘;
(5)为了防止溶液溅出,要用玻璃棒引流;洗涤烧杯并将洗涤液注入容量瓶的目的是将溶质都转移至容量瓶,故答案为:玻璃棒;将溶质全部转移至容量瓶;
(8)仰视刻度线,会导致溶液体积偏大,则浓度偏低,故答案为:偏低.
点评:本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.

练习册系列答案
相关题目
铁、铜混合粉末18.0g加入到100mL 5.0mol?L-1 FeCl3溶液中,充分反应后,剩余固体质量为2.8g.下列说法正确的是( )
| A、剩余固体是铁、铜混合物 |
| B、原固体混合物中铜的质量是9.6g |
| C、反应后溶液中n(Fe3+)=0.10mol |
| D、反应后溶液中n(Fe2+)+n(Cu2+)=0.75mol |
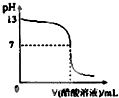 常温下,向10mL 0.1mol?L-1NaOH溶液中逐滴加入0.1mol?L-1醋酸溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,向10mL 0.1mol?L-1NaOH溶液中逐滴加入0.1mol?L-1醋酸溶液,所得滴定曲线如图所示.下列说法正确的是( )| A、pH=7时,所加醋酸溶液的体积为10mL |
| B、pH<7时,溶液中c(CH3COO-)<c(Na+) |
| C、醋酸滴入10ml时,c(Na+)═c(CH3COOH)+c(CH3COO-) |
| D、继续滴加0.1 mol?L-1醋酸溶液,溶液pH可以变为1 |
某氯碱厂利用废铁皮制取净水剂FeCl3溶液,最合理的生产途径是( )
A、Cl2
| |||||||||
B、Cl2
| |||||||||
C、Cl2
| |||||||||
D、 |
 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(g)(催化剂为Cu2O/ZnO):根据题意完成下列各题:
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(g)(催化剂为Cu2O/ZnO):根据题意完成下列各题: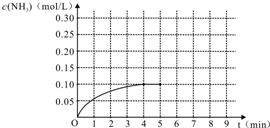 在容积为2L的密闭容器内加入0.4mol的N2和1.2mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)+Q(Q>0).反应中NH3的物质的量浓度随时间的变化情况如图:
在容积为2L的密闭容器内加入0.4mol的N2和1.2mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)+Q(Q>0).反应中NH3的物质的量浓度随时间的变化情况如图: