题目内容
A、B是两种常温下有刺激性气味的气体.将A、B分别通入品红溶液中,品红溶液均褪色.将A通入紫色石蕊试液中,溶液变为红色;将B通入紫色石蕊试液中,溶液先变红后褪色.将A和B按1:1的体积比充分混合,通入品红溶液中,品红溶液不褪色,通入紫色石蕊溶液中,溶液只变红不褪色.回答下列问题:
(1)写出A、B的化学式:A ;B ;
(2)写出A与NaOH溶液反应的化学方程式: 或
(3)加热通入A后变为无色的品红溶液,现象是 ;加热通入B后变为无色的品红溶液,现象是 .
(1)写出A、B的化学式:A
(2)写出A与NaOH溶液反应的化学方程式:
(3)加热通入A后变为无色的品红溶液,现象是
考点:常见气体的检验
专题:物质检验鉴别题
分析:具有漂白作用,能使品红溶液褪色的气体有Cl2、SO2、O3等,A气体通入紫色石蕊试液中,溶液只变红不褪色,所以A为SO2,将A(g)和B(g)按1:1的体积比混合充分,通入品红溶液中,品红溶液不褪色,则B为Cl2,发生下列反应:Cl2+SO2+2H2O═H2SO4+2HCl,生成的盐酸和硫酸都没有漂白作用,但它们只能使紫色石蕊试液变红色.
解答:
解:(1)具有漂白作用,能使品红溶液褪色的气体有Cl2、SO2、O3等,A气体通入紫色石蕊试液中,溶液只变红不褪色,所以A为SO2,将A(g)和B(g)按1:1的体积比混合充分,通入品红溶液中,品红溶液不褪色,则B为Cl2,故答案为:SO2;Cl2;
(2)二氧化硫为酸性气体,与NaOH反应生成Na2SO3或亚硫酸氢钠,反应的化学方程式为2NaOH+SO2=Na2SO3+H2O或NaOH+SO2=NaHSO3,故答案为:2NaOH+SO2=Na2SO3+H2O或NaOH+SO2=NaHSO3;
(3)二氧化硫具有漂白性,漂白原理是与有色物质发生化合反应生成不稳定的有色物质,不稳定,加热后能够复原,而氯气的漂白原理是由于氯气和水反应生成具有强氧化性的次氯酸,不能复原,故答案为:变为红色;无现象.
(2)二氧化硫为酸性气体,与NaOH反应生成Na2SO3或亚硫酸氢钠,反应的化学方程式为2NaOH+SO2=Na2SO3+H2O或NaOH+SO2=NaHSO3,故答案为:2NaOH+SO2=Na2SO3+H2O或NaOH+SO2=NaHSO3;
(3)二氧化硫具有漂白性,漂白原理是与有色物质发生化合反应生成不稳定的有色物质,不稳定,加热后能够复原,而氯气的漂白原理是由于氯气和水反应生成具有强氧化性的次氯酸,不能复原,故答案为:变为红色;无现象.
点评:本题考查氯气的性质,题目难度不大,本题注意氯气与二氧化硫的漂白性的区别.

练习册系列答案
相关题目
下列说法中不正确的是( )
| A、维生素C具有还原性,在人体内起抗氧化作用 |
| B、为防止月饼等富脂食品氧化变质,常在包装袋中放入硫酸亚铁 |
| C、由水电离出来的c(H+)=1×10-13mol/L的溶液中:K+、CO32-、Cl-、NO3-可能大量共存 |
| D、使石蕊变红的溶液中:Na+、I-、Cl-、NO3-可能大量共存 |
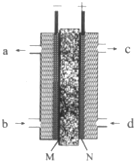 甲醇是燃料电池的常见原料,现已熔融的K2CO3为电解质,以甲醇为燃料,空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.如图是甲醇燃料电池模型,试回答下列问题:
甲醇是燃料电池的常见原料,现已熔融的K2CO3为电解质,以甲醇为燃料,空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.如图是甲醇燃料电池模型,试回答下列问题: 已知:H2(g)+
已知:H2(g)+