题目内容
3.以硫酸铜溶液作电解液,对含杂质Fe、Zn、Ag的粗铜进行电解精炼.下列叙述正确的是( )①粗铜与直流电源负极相连
②阴极发生的反应为Cu2++2e-=Cu
③电路中每通过3.0l×1023个电子,得到的精铜质量为16g
④杂质Ag以Ag2SO4的形式沉入电解槽形成“阳极泥”
| A. | ②③ | B. | ②④ | C. | ③④ | D. | ①③ |
分析 ①电解精炼粗铜时,粗铜作阳极、纯铜作阴极,阳极与电源正极相连、阴极与电源负极相连;
②阳极上金属材料失电子发生氧化反应、阴极上铜离子得电子发生还原反应;
③阳极上不仅铜失电子,比铜活泼的金属也失电子;
④杂质Zn失电子生成锌离子进入溶液,杂质Ag以单质形式进入溶液.
解答 解解:①电解精炼铜时,粗铜应作阳极,与直流电源正极相连,故①错误;
②阴极与电池的负极相连,是电解质中的阳离子发生还原反应,即Cu2++2e-═Cu,故②正确;
③根据电极反应:Cu2++2e-═Cu,电路中每通过3.01×1023个即0.5mol电子,得到的精铜质量为0.25mol×64g/mol=16g,故③正确;
④金属的活动性顺序为Zn>Fe>Cu>Ag>Pt,因此Ag、Pt不会放电,以单质形式沉积下来,故④错误;
故选:A.
点评 本题以电解精炼粗铜为载体考查电解原理,明确各个电极上发生的反应是解本题关键,知道阳极泥形成原理,注意:电解时,阳极材料是较活泼金属时,阳极上金属失电子而不是电解质溶液中阴离子失电子,为易错点.

练习册系列答案
相关题目
14.下列溶液中,有关离子一定能大量共存的是( )
| A. | 能使石蕊呈蓝色的溶液中:Na+、I-、Cl-、NO3- | |
| B. | 能使甲基橙呈黄色的溶液中:K+、SO32-、SO42-、ClO- | |
| C. | 能使pH试纸变蓝色的溶液中:Mg2+、Fe3+、NO3-、[Ag(NH3)2]+ | |
| D. | 能跟金属铝反应生成氢气的溶液中:NH4+、Al3+、Cl-、SO42- |
11.工业上常用煤和水作原料经过多步反应制得氢气,其中一步反应原理为:CO(g)+H2O(g)$\stackrel{催化剂}{?}$CO2(g)+H2(g),下面选项的条件中可判断该反应达到平衡状态的是( )
| A. | 单位时间内消耗1mol的H2O同时生成1mol的H2 | |
| B. | 两个H-O键断裂的同时有四个C-O键断裂 | |
| C. | 反应容器内的密度不再发生变化 | |
| D. | 混合气体的相对分子质量不发生变化 |
12.下列说法正确的是( )
| A. | 工业上常通过电解熔融的MgO冶炼金属镁 | |
| B. | 应用盖斯定律,可计算某些难以直接测量的反应焓变 | |
| C. | 用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1:2 | |
| D. | 已知:①2H2(g)+O2(g)=2H2O(g)△H=-aKJ/mol ②2H2(g)+O2(g)═2H2O(l)△H=-bKJ/mol△H1<△H2 |
13.下列实验装置能达到实验目的是(夹持仪器未画出)( )
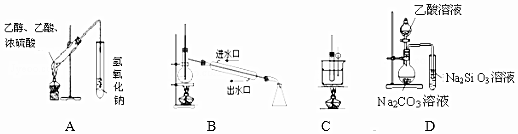

| A. | 装置用于制备乙酸乙酯 | |
| B. | 装置用于石油的分馏 | |
| C. | 装置用于实验室制硝基苯 | |
| D. | 装置可装置证明酸性:乙酸>碳酸>硅酸 |