题目内容
1.在一个密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol/L、0.2 mol/L、0.2 mol/L,当反应达到反应限度时可能的数据是( )| A. | c(SO3)=0.4 mol/L | B. | c(SO2)=c(SO3)=0.15 mol/L | ||
| C. | c(O2)=0.35 mol/L | D. | c(SO2)+c(SO3)=0.4 mol/L |
分析 对于反应2SO2(g)+O2(g)?2SO3(g),某一时刻SO2、O2、SO3物质的量浓度分别为0.2mol/L、0.2mol/L、0.2mol/L,可利用极限转化分析各物质的最大浓度,但由于反应为可逆反应,则各物质的浓度一定小于最大浓度,以此来解答.
解答 解:2SO2(g)+O2(g)?2SO3(g),
某时刻0.2mol/L 0.2mol/L 0.2mol/L
极限转化0.4mol/L 0.3mol/L 0
极限转化 0 0.1mol/L 0.4mol/L
A.由于反应为可逆反应,SO3的浓度一定小于0.4mol/L,故A错误;
B.SO3、SO2浓度不会均为0.15mol/L,只能一种物质的浓度增大,另一种物质的浓度减小,故B错误;
C.由于反应为可逆反应,O2的浓度一定小于0.3mol/L,则不可能为0.35mol/L,故C错误;
D.根据元素守恒定律,c(SO2)+c(SO3)=0.4mol/L,故D正确.
故选D.
点评 本题考查可逆反应,注意可逆反应的特点为不完全转化性,学生应学会利用极限转化的思想来分析物质的最大浓度,但实际浓度一定小于最大浓度,难度不大.

练习册系列答案
相关题目
11.某化学兴趣小组的成员捡到一块矿石,观察外观发现该矿石坚硬且呈红褐色,投入水中没有任何变化,再向水中加浓盐酸至过量,矿石部分溶解,并有大量无色气体生成.学生猜测该矿石可能由CaCO3、SiO2、Fe2O3三种成分组成,试设计实验证明CaCO3以外的两种成分.
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、滴管、药匙、漏斗、漏斗架;2 mol•L-1盐酸、2mol•L-1NaOH溶液、2%的KSCN溶液.
(1)将实验方案用以下流程示意图表示,试写出每步所用试剂的名称或化学式.
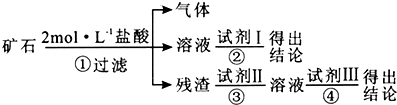
试剂Ⅰ2%的KSCN溶液;试剂Ⅱ2mol•L-1NaOH溶液;试剂Ⅲ2mol•L-1盐酸.
(2)如果猜测是成立的,试根据上述实验方案,叙述实验操作,预期现象和结论.
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、滴管、药匙、漏斗、漏斗架;2 mol•L-1盐酸、2mol•L-1NaOH溶液、2%的KSCN溶液.
(1)将实验方案用以下流程示意图表示,试写出每步所用试剂的名称或化学式.

试剂Ⅰ2%的KSCN溶液;试剂Ⅱ2mol•L-1NaOH溶液;试剂Ⅲ2mol•L-1盐酸.
(2)如果猜测是成立的,试根据上述实验方案,叙述实验操作,预期现象和结论.
| 编号 | 实验操作 | 预期现象和结论 |
| ① | 取适量矿石研细,加 足量2 mol•L-1盐酸 | 有大量无色气体生成,得棕黄 色溶液,且仍有少量固体残留 |
| ② | ||
| ③ | ||
| ④ |
12. 镁、铝、锌是生活中常见的三种金属,查阅资料获得如下信息:
镁、铝、锌是生活中常见的三种金属,查阅资料获得如下信息:
①镁、铝、锌都是银白色的金属
②锌(Zn)可以与NaOH溶液反应生成H2
③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3•H2O
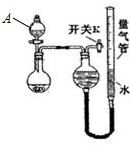
④Zn2+易形成配合物如[Zn(NH3)4]2+,该配合物遇强酸分解生成Zn2+、NH4+(1)(1)甲同学取镁铝合金进行定量分析,用图所示装置进行实验,获得如下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
(2)乙同学取镁铝锌合金设计如下实验方案:
(可用试剂:样品、pH试纸、稀硫酸、NaOH溶液、氨水)
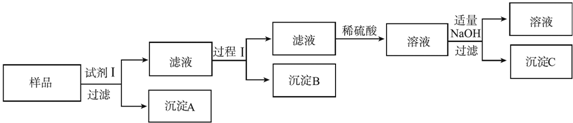
①试剂Ⅰ是NaOH溶液;沉淀B是Al(OH)3.
②过程Ⅰ是:在滤液中逐滴加入稀硫酸,直至生成的沉淀刚好溶解,再加入足量的稀氨水,过滤.
③沉淀C与氨水反应的离子方程式为Zn(OH)2+4NH3=[Zn(NH3)4]2++2OH-;或Zn(OH)2+4NH3•H2O=[Zn(NH3)4]2++2OH-+4H2O.
 镁、铝、锌是生活中常见的三种金属,查阅资料获得如下信息:
镁、铝、锌是生活中常见的三种金属,查阅资料获得如下信息:①镁、铝、锌都是银白色的金属
②锌(Zn)可以与NaOH溶液反应生成H2
③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3•H2O
④Zn2+易形成配合物如[Zn(NH3)4]2+,该配合物遇强酸分解生成Zn2+、NH4+(1)(1)甲同学取镁铝合金进行定量分析,用图所示装置进行实验,获得如下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
| 编号 | 粉末质量 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 2.0 g | 10.0 mL | 346.2 mL |
| ② | 2.0 g | 10.0 mL | 335.0 mL |
| ③ | 2.0 g | 10.0 mL | 345.8 mL |
(可用试剂:样品、pH试纸、稀硫酸、NaOH溶液、氨水)

①试剂Ⅰ是NaOH溶液;沉淀B是Al(OH)3.
②过程Ⅰ是:在滤液中逐滴加入稀硫酸,直至生成的沉淀刚好溶解,再加入足量的稀氨水,过滤.
③沉淀C与氨水反应的离子方程式为Zn(OH)2+4NH3=[Zn(NH3)4]2++2OH-;或Zn(OH)2+4NH3•H2O=[Zn(NH3)4]2++2OH-+4H2O.
9.铁的常见化合价有+2和+3.据研究,铁在浓HNO3中发生钝化时,可生成一种化学式为Fe8O11的化合物,它可以看作由FeO和Fe2O3组成的复杂氧化物.该化合物可以表示为( )
| A. | FeO•3Fe2O3 | B. | 2FeO•3Fe2O3 | C. | FeO•2Fe2O3 | D. | 2FeO•Fe2O3 |
6. 现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题:
现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题:
(1)写出C、D、E三种原子第一电离能由大到小的顺序为F>N>O.(用元素符号表示)
(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为H2O>NH3>CH4(用分子式表示),根据价层电子对互斥理论预测BA2D的分子构型为平面三角形.
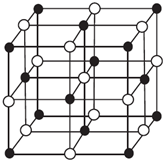
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据六面体互不相邻的顶点,而六面体的每条棱上均有一个BC-.与A同族且相隔两个周期的元素R的离子位于立方体的恰当位置上.根据其结构特点可知该晶体的化学式为(用最简正整数表示)KFe2(CN)6.
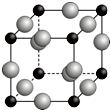
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
根据表格中的数据:判断KCl、MgO、TiN 三种离子晶体熔点从高到低的顺序是TiN>MgO>KCl.MgO晶体中一个Mg2+周围和它最邻近且等距离的O2-有6个.
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是Cr2O3.
 现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题:
现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题:(1)写出C、D、E三种原子第一电离能由大到小的顺序为F>N>O.(用元素符号表示)
(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为H2O>NH3>CH4(用分子式表示),根据价层电子对互斥理论预测BA2D的分子构型为平面三角形.
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据六面体互不相邻的顶点,而六面体的每条棱上均有一个BC-.与A同族且相隔两个周期的元素R的离子位于立方体的恰当位置上.根据其结构特点可知该晶体的化学式为(用最简正整数表示)KFe2(CN)6.
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是Cr2O3.
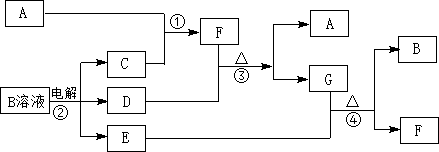 (1)写出化学式FNH3,
(1)写出化学式FNH3,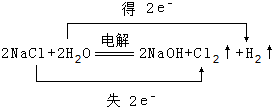 .
. 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn+1;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层电子数与B的相同,其余各内层轨道均充满电子.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大.其中基态A原子价电子排布式为nsnnpn+1;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层电子数与B的相同,其余各内层轨道均充满电子.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):