题目内容
10.下列说法错误的是( )| A. | 向苦卤(含K+、Mg2+、Br-等)中通入Cl2是为了提取溴 | |
| B. | 粗盐(含Ca2+、Mg2+、SO42-、泥沙等杂质)可采用除杂和重结晶等过程提纯 | |
| C. | 海带提碘只涉及物理变化,海水提镁涉及复分解反应 | |
| D. | 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收 |
分析 A.氯气可氧化溴离子生成溴单质;
B.过滤可除去泥沙,需要化学试剂将Ca2+、Mg2+、SO42-转化为沉淀再过滤,对滤液结晶得到NaCl;
C.碘以离子形式存在,海水在镁离子需要转化为氯化镁,电解熔融氯化镁制备Mg;
D.用空气和水蒸气吹出单质溴,再用SO2将其还原吸收转化为HBr,达到富集的目的.
解答 解:A.向苦卤中通入Cl2置换出溴单质,分离得到溴,通入Cl2是为了提取溴,故A正确;
B.粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时通常在溶液中依次中加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性,再进行重结晶进行提纯,故B正确;
C.海带提碘、海水提镁均涉及氧化还原反应,故C错误;
D.海水提取溴一般用氯气置换溴离子转化为溴单质,用空气和水蒸气吹出单质溴,再用SO2将其还原吸收转化为HBr,达到富集的目的,故D正确;
故选C.
点评 本题考查海水资源的应用,为高频考点,把握元素的存在形式、发生的反应、混合物分离提纯为解答的关键,侧重分析与应用能力的考查,注意化学与生活的联系,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.将3.84g铜粉与一定质量的浓硝酸反应,当铜完全作用时,收集到气体2.24L(标准状况下),则所消耗硝酸的物质的量( )
| A. | 0.24mol | B. | 0.22mol | C. | 0.16mol | D. | 0.1mol |
18.下列溶液一定呈中性的是( )
| A. | c(H+)=c(OH-)=1×10-6mol•L-1的溶液 | |
| B. | 等物质的量的强酸和强碱反应后所得到的混合溶液 | |
| C. | 将pH=5的盐酸稀释100倍所得到的溶液 | |
| D. | 非电解质溶于水得到的溶液 |
15.下列变化中需要加入还原剂才能发生的是( )
| A. | N2→NO | B. | N2→NH3 | C. | NO→NO2 | D. | NH3→NO |
2.下列属于置换反应的是( )
| A. | 2KI+Cl2=2KCl+I2 | B. | CaCO3=CaO+CO2↑ | ||
| C. | SO3+H2O=H2SO4 | D. | MgCl2+2NaOH=Mg(OH)2↓+NaCl |
19.下列各分子中,所有原子都满足最外层8电子稳定结构的是( )
| A. | H2O | B. | BF3 | C. | CCl4 | D. | LiCl |
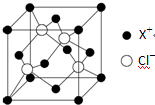
 元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子.在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2XCl+2CO+2H2O═X2Cl2•2CO•2H2O
元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子.在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2XCl+2CO+2H2O═X2Cl2•2CO•2H2O