题目内容
将3.5g Mg、Fe合金投入一定量的硝酸中,金属与硝酸恰好完全反应,共收集到标况下的气体V L(HNO3被还原为NO和NO2),若向反应后的溶液中加入足量的NaOH溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、干燥后称量,质量为8.6g,求收集到气体体积V值范围.
考点:化学方程式的有关计算
专题:计算题
分析:得到的沉淀是铁的氢氧化物和Mg(OH)2的混合物,质量增加量就是结合的OH-的质量,计算氢氧根的物质的量,由电荷守恒可知,金属提供电子物质的量等于沉淀中氢氧根的物质的量,采用极值法计算:假设全是NO或全是NO2,根据电子转移守恒计算气体物质的量,再根据V=nVm计算生成气体体积,实际混合气体体积应介于二者之间.
解答:
解:得到的沉淀是铁的氢氧化物和Mg(OH)2的混合物,质量增加量就是结合的OH-的质量,所以m(OH-)=8.6gg-3.5g=5.1g,因此 n(OH-)=
=0.3 mol,由电荷守恒可知,金属提供电子物质的量等于沉淀中氢氧根的物质的量,即Fe、Mg共失去0.3 mol电子,
假设得到的气体全是NO,由电子转移守恒可知,则n(NO)=
=0.1mol,所以NO体积是:0.1 mol×22.4 L/mol=2.24 L,
假设得到的气体全是NO2,由电子转移守恒可知,则n(NO2)=
=0.3mol,所以NO2体积是:0.3 mol×22.4 L/mol=6.72 L,
因为得到是混合气体,因此混合气体的体积应介于二者之间,即2.24<V<6.72,
答:收集到气体体积V值范围为:2.24<V<6.72.
| 5.1g |
| 17g/mol |
假设得到的气体全是NO,由电子转移守恒可知,则n(NO)=
| 0.3mol |
| 3 |
假设得到的气体全是NO2,由电子转移守恒可知,则n(NO2)=
| 0.3mol |
| 1 |
因为得到是混合气体,因此混合气体的体积应介于二者之间,即2.24<V<6.72,
答:收集到气体体积V值范围为:2.24<V<6.72.
点评:本题考查了混合物计算,难度中等,利用守恒思想计算,避免难以确定Fe反应后的价态,关键是确定氢氧根离子所带电荷等于金属失去的电子.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
根据右表提供的数据,判断在等物质的量浓度的NaClO和NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| 化学式 | 电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K1=4.4×10-7K2=4.7×10-11 |
| A、c(H+)+c(H2CO3)═c(OH-)+c(CO32-) |
| B、c(Na+)>c(ClO-)>c(HCO3-) |
| C、c(HClO)+c(ClO-)═c(HCO3-)+c(CO32-)+c(H2CO3) |
| D、c(Na+)+c(H+)═c(HCO3-)+c(ClO-)+c(OH-)+c(CO32-) |
化学键的断裂和形成的观点不能用于解释下列事实中的( )
| A、物质三态变化 |
| B、化学反应的能量变化 |
| C、加成反应 |
| D、化学反应的物质变化 |
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Z为地壳中含量最高的金属元素.下列说法正确的是( )
| X | ||||||
| Y | Z | W |
| A、工业上电解YW饱和溶液冶炼金属Y |
| B、气态氢化物的稳定性:W>X |
| C、简单离子半径的大小顺序:r(Y+)>r(X-) |
| D、Y、W的最高价氧化物的水化物均能溶解金属Z |
将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应2A ( g)+B(g)?2C(g),若经2s后测得C的浓度为0.6mol/L,现有下列几种说法,其中正确的是( )
| A、用物质A表示的反应的平均速率为0.3 mol?L-1?s-1 |
| B、用物质B表示的反应的平均速率为0.6 mol?L-1?s-1 |
| C、2 s时物质A的转化率为70% |
| D、2 s时物质B的浓度为0.3 mol/L |
将0.1mol/L稀氨水加水稀释,下列说法正确的是( )
| A、溶液中c(H+)和c(OH-)都减小 |
| B、溶液中c(H+)增大 |
| C、NH3?H2O电离平衡向左移动 |
| D、溶液pH增大 |
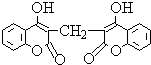 某农民偶然发现他的一头小母牛食用腐败草料后,血液不会凝固.化学家由此得到启发,从腐败草料中提取出结构简式为如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )
某农民偶然发现他的一头小母牛食用腐败草料后,血液不会凝固.化学家由此得到启发,从腐败草料中提取出结构简式为如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )| A、有望将它发展制得一种抗凝血药 |
| B、它无嗅并略具芳香味,因而可用来制备致命性出血型的杀鼠药 |
| C、它可由化合物和甲醛(HCHO)通过缩合反应制得 |
| D、它易溶于水、乙醇、乙醚等有机溶剂 |
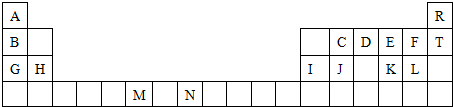
 所示,该晶胞中含有金属原子的数目为
所示,该晶胞中含有金属原子的数目为