题目内容
10.NA 表示阿伏伽德罗常数,下列叙述正确的是( )| A. | 实验室用浓盐酸与MnO2反应制Cl2,每生成22.4 LCl2,转移的电子总数为2NA | |
| B. | 1 mol O2在反应中作氧化剂时,所得电子数一定为4NA | |
| C. | 1 mol Na2O2与足量H2O反应,转移电子数为2NA | |
| D. | 0.1 mol金属钠在过量氧气中充分燃烧,生成的化合物中离子总数为0.15NA |
分析 A、氯气所处的状态不明确;
B、氧气反应后的价态不明确;
C、过氧化钠和水反应时,1mol过氧化钠转移1mol电子;
D、钠在氧气中燃烧生成过氧化钠,而在过氧化钠中含2个钠离子和1个过氧根.
解答 解:A、氯气所处的状态不明确,故氯气的物质的量无法计算,则转移的电子数无法计算,故A错误;
B、氧气反应后的价态不明确,故氧气得到的电子数无法计算,故B错误;
C、过氧化钠和水反应时,1mol过氧化钠转移1mol电子,即转移NA个电子,故C错误;
D、钠在氧气中燃烧生成过氧化钠,0.1mol钠反应生成0.05mol过氧化钠,而在过氧化钠中含2个钠离子和1个过氧根,故0.05mol过氧化钠中含0.15NA个离子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
20.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,22.4 L CCl4、CO2含有的分子数为NA | |
| B. | 通常状况下,NA个CO2分子占有的体积约为22.4 L | |
| C. | 常温常压下,1.06 g Na2CO3含有的Na+离子数为0.02NA | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA |
1.下列离子方程式正确的是( )
| A. | 盐酸与氢氧化钠溶液反应:H++OH-═H2O | |
| B. | 碳酸钙与稀硝酸的反应:CO32-+2H+═CO2+H2O | |
| C. | 铜与稀硫酸反应:Cu+2H+═Cu2++H2↑ | |
| D. | 氯气与氢氧化钠溶液反应:Cl2+OH-═Cl-+ClO-+H2O |
5.用食用白醋(醋酸浓度约1mol•L-1)进行下列实验,能证明醋酸为弱电解质的是( )
| A. | 白醋中滴入石蕊试液呈红色 | B. | 白醋加入热水瓶中除去水垢 | ||
| C. | 蛋壳浸泡在白醋中有气体放出 | D. | pH试纸显示白醋的pH为2~3 |
15.对于工业合成氨反应:N2+3H2?2NH3,下列说法错误的是( )
| A. | 使用合适的催化剂可以加大反应速率 | |
| B. | 升高温度可以增大反应速率 | |
| C. | 增大N2浓度可以使H2转化率达到100% | |
| D. | 增大N2浓度可以减小反应速率 |
4.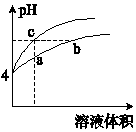 某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示.下列判断正确的是( )
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示.下列判断正确的是( )
 某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示.下列判断正确的是( )
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示.下列判断正确的是( )| A. | a、c两点溶液的导电能力相同 | |
| B. | a、b、c三点溶液中水的电离程度:a>b>c | |
| C. | b点溶液中:c(H+)+c(NH3•H2O)=c(OH-) | |
| D. | 用NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液的体积Vb=Vc |
 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: