题目内容
11.室温下,下列各组离子在指定溶液中能大量共存的是( )| A. | 饱和氯水中 Cl-、$NO_3^-$、Na+、$SO_3^{2-}$ | |
| B. | c(H+)=1.0×10-13mol•L-1溶液中 ${C_6}{H_5}{O^-}$、K+、$SO_4^{2-}$、Br- | |
| C. | Na2S溶液中 $SO_4^{2-}$、K+、Cl-、Cu2+ | |
| D. | pH=12的溶液中 $NO_3^-$、I-、Na+、Al3+ |
分析 A.亚硫酸根离子具有还原性,能够被氯水氧化;
B.该溶液中存在大量氢氧根离子,四种离子之间不反应,都不与企业广告离子反应;
C.硫化钠与铜离子反应生成难溶物硫化铜;
D.该溶液呈碱性,铝离子与氢氧根离子反应.
解答 解:A.饱和氯水中的氯气分子能将SO32-氧化,在溶液中不能大量共存,故A错误;
B.c(H+)=1×10-13mol•L-1溶液呈碱性,C6H5O-、K+、SO42-、Br-离子之间不反应,都不与氢氧根离子反应,可以大量共存,故B正确;
C.硫化钠与Cu2+发生反应:Cu2++S2-=CuS↓,在溶液中不能大量共存,故C错误;
D.pH=12的溶液呈碱性,Al3+与氢氧根离子反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.对于某些离子的检验及结论中一定正确的是( )
| A. | 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,则一定有SO42- | |
| C. | 用NaOH溶液能鉴别Mg( NO3)2、Cu( NO3)2和NaNO3三种溶液 | |
| D. | 加入硝酸银溶液后产生白色沉淀,再加盐酸,白色沉淀不消失,一定有Cl- |
2.下列说法不正确的是( )
| A. | 电解熔融的氯化钠中铁电极连接电源的负极 | |
| B. | 电解熔融的氯化钠中石墨电极作阳极发生氧化反应 | |
| C. | 可用电解饱和氯化钠溶液来制备金属钠 | |
| D. | 熔融氯化钠的电离是在电流的作用下发生的 |
6.在密闭容器中进行反应:X2(g)+Y2(g)?2Z(g)已知X2、Y2、Z的起始浓度分别为0.1mol•L-1、0.3mol•L-1、0.2mol•L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A. | Y2为0.15mol/L | B. | Z为0.2mol/L | C. | X2为0.3mol/L | D. | Z为0.4mol/L |
16.X、Y、Z、W、R均为短周期主族元素,原子序数依次增加,X与W、Y与R分别同主族.Z在短周期元素中金属性最强,W元素原子的次外层电子数为最外层电子数的2倍,R的原子序数是Y的2倍.下列叙述错误的是( )
| A. | 原子半径:W>X>Y | |
| B. | 最高价氧化物对应水化物的酸性强弱:R>W>X | |
| C. | Y的氢化物比R的氢化物稳定,熔沸点高 | |
| D. | Y与Z形成的两种化合物中阴、阳离子的个数比均为1:2 |
3.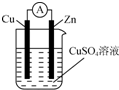 将锌棒和铜棒按图示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )
将锌棒和铜棒按图示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )
 将锌棒和铜棒按图示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )
将锌棒和铜棒按图示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )| A. | 该装置是将电能转化为化学能 | |
| B. | 锌棒为正极 | |
| C. | 电子由铜棒流出 | |
| D. | 该电池总反应为Zn+CuSO4═ZnSO4+Cu |
20.能证明某溶液中含有Fe2+的是( )
| A. | 该溶液呈浅绿色 | |
| B. | 该溶液中加入NaOH溶液,生成白色沉淀并迅速变成灰绿色,最终变为红褐色 | |
| C. | 向该溶液中加入氯水,再滴入几滴KSCN溶液,呈红色 | |
| D. | 向该溶液中滴入几滴KSCN溶液,不变色,再加入氯水,有红色沉淀生成 |
 原子序数依次递增且都小于36的X、Y、Z、Q、W四种元素,其中X是原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Q原子基态时2p原子轨道上有2个未成对的电子,W元素的原子结构中3d能级有4个未成对电子.回答下列问题:
原子序数依次递增且都小于36的X、Y、Z、Q、W四种元素,其中X是原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Q原子基态时2p原子轨道上有2个未成对的电子,W元素的原子结构中3d能级有4个未成对电子.回答下列问题: